
【题目】实验室合成氨装置如图所示,则以下说法中错误的是( )
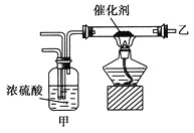
A.装置甲的作用之一是干燥
B.装置甲的作用是化合
C.乙处导出的气体是N2、H2、NH3
D.检验产物可用湿润的红色石蕊试纸或浓盐酸等
科目:高中化学 来源: 题型:
【题目】已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:
NaCN+HNO2![]() HCN+NaNO2 NaCN+HF
HCN+NaNO2 NaCN+HF![]() HCN+NaF NaNO2+HF
HCN+NaF NaNO2+HF![]() HNO2+NaF
HNO2+NaF
由此可判断下列叙述不正确的是
A.K(HF)=7.2×10-4B.K(HNO2)=4.9×10-10
C.根据两个反应即可得出结论D.K(HCN)<K(HNO2)<K(HF)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为 ( )
A.9.02gB.8.26gC.8.51gD.7.04g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备甲基丙烯酸甲酯的反应装置如图所示,有关信息如下:
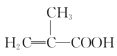 +CH3OH
+CH3OH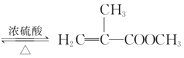 +H2O
+H2O

已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;CaCl2可与醇结合形成复合物。
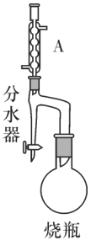
实验步骤:
①向100mL烧瓶中依次加入:15mL甲基丙烯酸、2粒沸石、10mL无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热烧瓶。在反应过程中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当____,停止加热;
④冷却后用试剂X洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。
请回答下列问题:
(1)A装置的名称是__。
(2)请将步骤③填完整__。
(3)上述实验可能生成的副产物结构简式为__(填两种)。
(4)下列说法正确的是___(填字母代号)。
A.在该实验中,浓硫酸是催化剂和脱水剂
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和Na2CO3、饱和CaCl2溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
(5)实验结束收集分水器分离出的水,并测得质量为2.70g,计算甲基丙烯酸甲酯的产率约为__(结果保留一位小数)。实验中甲基丙烯酸甲酯的实际产率总是小于此计算值,可能其原因不是__(填字母代号)。
A.分水器收集的水里含甲基丙烯酸甲酯
B.实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、X是中学化学中常见的四种物质,且a、b、c中含有同一种元素,其转化关系如下图所示。下列说法不正确的是

A. 若a、b、c均为厨房中常用的物质,则构成c中的阳离子半径小于其阴离子半径
B. 若a为一种气态氢化物,X为O2,则a分子中可能含有10个或者18个电子
C. 若b为一种两性氢氧化物,则X可能是强酸,也可能是强碱
D. 若a为固态非金属单质,X为O2,则O元素与a元素的原子序数之差可能为8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:N2(g)+3H2(g) ![]() 2NH3(g) △H<0,2SO2(g)+O2(g)
2NH3(g) △H<0,2SO2(g)+O2(g)![]() 2SO3(g) △H<0。请回答下列问题:
2SO3(g) △H<0。请回答下列问题:
(1)从影响化学反应速率和化学平衡的因素分析,要有利于NH3和SO3的生成,理论上应采取的措施是_______。实际生产中采取的措施是_________。
(2)在合成氨的工业生产中,要分离出氨,目的是__________;而合成SO3的过程中,则不需要分离出SO3,原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小
B.物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的
C.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全
D.除去溶液中Mg2+,用OH-比![]() 效果好,说明Mg(OH)2的溶解度比MgCO3小
效果好,说明Mg(OH)2的溶解度比MgCO3小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2008年10月8日,瑞典皇家科学院宣布将诺贝尔化学奖授予日本科学家下村修、美国科学家马丁沙尔菲与美籍华裔科学家钱永健,以表彰三人因在发现和研究绿色荧光蛋白方面做出的贡献。蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量[约在14%~18%(本题涉及的含量均为质量分数)],故食品中蛋白质的含量测定常用凯氏定氮法,其测定原理是:
Ⅰ.蛋白质中的氮(用氨基表示)在强热和CuSO4、浓H2SO4作用下,生成一种无机含氮化合物,反应式为:2(-NH2)+H2SO4+2H+![]() ;
;
Ⅱ.该无机化合物在凯氏定氮器中与碱作用,通过蒸馏释放出NH3,收集于H3BO3溶液中,生成(NH4)2B4O7;
Ⅲ.用已知浓度的HCl标准溶液滴定,根据HCl消耗的量计算出氮的含量,然后乘以相应的换算系数,即得蛋白质的含量。
(1)上述原理第Ⅰ步生成的无机含氮化合物化学式为_________;
(2)乳制品的换算系数为6.38,即若检测出氮的含量为1%,蛋白质的含量则为6.38%.不法分子通过在低蛋白含量的奶粉中加入三聚氰胺(Melamine)来“提高”奶粉中的蛋白质含量,导致许多婴幼儿肾结石。
①三聚氰胺的结构如图所示,其化学式为_________,含氮量(氮元素的质量分数)为_________;
②下列关于三聚氰胺的说法中,正确的有_________;
A.三聚氰胺是一种白色结晶粉末,无色无味,所以掺入奶粉后不易被发现
B.三聚氰胺分子中所有原子可能在同一个平面上
C.三聚氰胺呈弱碱性,可以和酸反应生成相应的盐
③假定奶粉中蛋白质含量为16%即为合格,不法分子在一罐总质量为500g、蛋白质含量为0的假奶粉中掺入_________g的三聚氰胺就可使奶粉“达标”。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种磁性材料的磨削废料(含镍质量分数约21%)主要成分是铁镍合金,还含有铜、钙、镁、硅的氧化物。由该废料制备纯度较高的氢氧化镍,工艺流程如下:
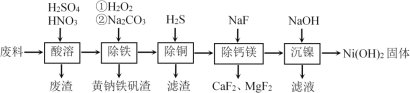
回答下列问题:
(1)合金中的镍难溶于稀硫酸,“酸溶”时除了加入稀硫酸,还要边搅拌边缓慢加入稀硝酸,反应有N2生成。写出金属镍溶解的离子方程式________________________。
(2)“除铁”时H2O2的作用是____________________,为了证明添加的H2O2已足量,应选择的试剂是____________________(填“铁氰化钾”或“硫氰化钾”)溶液。黄钠铁矾[NaxFey(SO4)m(OH)n]具有沉淀颗粒大、沉淀速率快、容易过滤等特点,则x∶y∶m∶n=1∶3∶2∶________。
(3)“除铜”时,反应的离子方程式为_________________________,若用Na2S或Na2S2O3代替H2S除铜,优点是__________________________。
(4)已知除杂过程在陶瓷容器中进行,NaF的实际用量为理论用量的1.1倍,用量不宜过大的原因是_______________________________。
(5)100kg废料经上述工艺制得Ni(OH)2固体的质量为31kg,则镍回收率的计算式为_______。
(6)镍氢电池已成为混合动力汽车的主要电池类型,其工作原理如下:M+Ni(OH)2![]() HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
HM+NiOOH(式中M为储氢合金)。写出电池放电过程中正极的电极反应式________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com