
����Ŀ�����¶�T1��T2ʱ���ֱ�0.50 mol CH4��1.2mol NO2����1 L���ܱ������з�����Ӧ��
CH4��g����2NO2��g��![]() N2��g����CO2��g����2H2O��g����H=akJ/mol������й��������±���
N2��g����CO2��g����2H2O��g����H=akJ/mol������й��������±���
�¶� | ʱ��/min ���ʵ��� | 0 | 10 | 20 | 40 | 50 |
T1 | n��CH4��/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n��CH4��/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
����˵����ȷ����
A��T1��T2����a��0
B�����¶�ΪT2����Ӧ���е�40 minʱ�� x��0.15
C���¶�ΪT2ʱ������ƽ�����������ٳ���0.50 mol CH4��1.2mol NO2�����´ﵽƽ��ʱ��n��N2��=0.70mol
D���¶�ΪT1ʱ����ƽ��ʱCH4 ��ת���ʴ���NO2��ת����
���𰸡�D
��������
���������A���¶����ߣ���Ӧ���ʼӿ죬���T2��T1������ʣ�������࣬˵����Ӧ������У�����Ӧ���ȣ�����a��0����A����B�����¶�ΪT2����Ӧ���е�40 minʱ����Ӧ�ﵽƽ��״̬��x=0.15����B����C���¶�ΪT2ʱ������ƽ�����������ٳ���0.50 mol CH4��1.2mol NO2��ƽ�������ƶ������´ﵽƽ��ʱ��n��N2��С��ԭƽ��n��N2����2������C����D���¶�ΪT1ʱ����ƽ��ʱCH4 ��ת����Ϊ��0.50-0.10��mol��0.50mol��100%=80%��NO2��ת����Ϊ��0.50-0.10����2mol��1.20mol��100%=66.7%����D��ȷ����ΪD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ijѧ���Ļ�ѧʵ�鱨���������¼�¼����ʵ�����ݺ����ģ� ��
A. ��100 mL��Ͳ��ȡ5.26 mLϡ������Һ
B. ��������ƽ��ȡ11.7 g CuO��ĩ
C. �ù㷺pH��ֽ�����Һ��pHΪ3.5
D. �¶ȼ�����ʾ�����¶���Ϊ25.68oC
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z��ԭ�������������ӣ�m��p��r������ЩԪ����ɵĶ�Ԫ�����n��Ԫ��Z�ĵ��ʣ�ͨ��Ϊ����ɫ���壬q��ˮ��Һ����Ư���ԣ�0.01mol/L r��Һ��pHΪ2��p�Ǽ��飬�������ʵ�ת����ϵ��ͼ��ʾ������˵����ȷ����
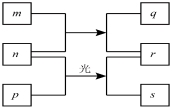
A��X������������Ӧ��ˮ����Ϊ����
B��Ԫ�صķǽ�����Z��X��Y
C��Y���⻯�ﳣ�³�ѹ��Ϊ��̬
D��ԭ�Ӱ뾶�Ĵ�СW��X��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������
A. �����к���̼������ʴ�����ȴ�����
B. �������ӵ��������������Ӵ�������
C. ������Ʒ�϶�ͭʱ���Ƽ�Ϊ������ͭ��Ϊ���Һ
D. ��������Ƕп�飬���ܲ��ױ���ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�Ԫ�����ڱ���˵������ȷ���ǣ� ��
A.��15��ijԪ�����γɼ�������
B.��2��Ԫ���п϶�û�зǽ���Ԫ��
C.��17�еĵ�һ��Ԫ�ص�ԭ������Ϊ8
D.������������ǿ�Ӧ����H2�Ľ���Ԫ��λ�ڵڢ�A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������ȤС���H2O2�ķֽ�������������ʵ��̽����
��1���±��Ǹ�С���о�Ӱ�����������H2O2���ֽ����ʵ�����ʱ�ɼ���һ�����ݣ�
��10 mL H2O2��ȡ150 mL O2�����ʱ��
Ũ�� ʱ�������� ��Ӧ���� | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
������������������ | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ | ���� ����Ӧ |
���������������� | 360 | 480 | 540 | 720 |
������MnO2���������� | 10 | 25 | 60 | 120 |
��С������Ʒ���ʱ��������Ũ�ȡ�a��___________b��___________�����ضԹ�������ֽ����ʵ�Ӱ�졣
��������Ӱ��H2O2�ֽ����ʵ�����a��b����ѡһ����˵�������ضԸ÷�Ӧ���ʵ�Ӱ�죺_____________��
��2����������ͬ��������С��ͬ��MnO2�ֱ���뵽5 mL 5%��˫��ˮ�У����ô����ǵ�ľ�����ԡ��ⶨ������£�
���� ��MnO2�� | ������� | �۲��� | ��Ӧ��������ʱ�� |
��ĩ״ | ��ϲ��� | ���ҷ�Ӧ�������ǵ�ľ����ȼ | 3.5���� |
��״ | ��Ӧ���������Ǻ�����ľ��δ��ȼ | 30���� |
��д��H2O2������Ӧ�Ļ�ѧ����ʽ��______________________��
��ʵ����˵���������õĴ�С��________________�йء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ��Ӧ�����ӷ���ʽ��ȷ����
A�����ˮ�еμ�FeCl3��Һ�Ʊ�Fe(OH)3���壺Fe3+��3H2O![]() Fe(OH)3����3H+
Fe(OH)3����3H+
B����FeCl3��Һ�м���Cu�ۣ�2Fe3++Cu=2Fe2++Cu2+
C��̼������Һ��ʯ����ķ�Ӧ��CO32-��Ca2+=CaCO3��
D������������Һ��ϡ���ᷴӦ��Ba2++SO42-+H++OH-=BaSO4��+H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. Һ���ӷ����ڴ��Һ����Լ�ƿ��Ӧ��ˮ��
B. ��ʹʪ��ĵ���KI��ֽ����ɫ������һ����Cl2
C. ij��Һ�м���CCl4��CCl4������ɫ��֤��ԭ��Һ�д���I��
D. �к͵ζ�ʵ��ʱ���ô���Һ��ϴ��ƿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ������ƿ�����ȣ���ͬ�¡�ͬѹʱƿ������Ĺ�ϵһ����ȷ����
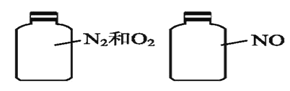
A������ԭ������� B�������ܶ����
C������������� D��Ħ���������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com