
| A、22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| B、常温下,1L O.1mol/L NH4NO3的溶液中含氮原子数为0.2NA |
| C、室温下,21.Og乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
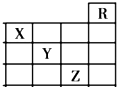 如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是( )
如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述正确的是( )| A、只有③ | B、只有①④ |
| C、只有①②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z与Y两种元素组成的化合物中,阴、阳离子个数比为1:1或1:2 |
| B、Y、Z、W元素形成的简单离子具有相同电子层结构,其离子半径依次增大 |
| C、Z、R元素的氧化物的水化物之间相互反应生成的盐溶液呈中性、碱性或酸性 |
| D、Y、R元素分别与X元素形成的化合物的沸点:XmY<XmR |
查看答案和解析>>
科目:高中化学 来源: 题型:
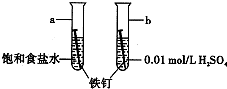 如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )
如图是研究铁钉腐蚀的装置图.下列说法不正确的是( )| A、ab在两处的腐蚀速率a<b |
| B、a、b两处铁钉中的碳均为正极 |
| C、a、b两处铁钉中的铁均失电子被氧化 |
| D、a、b两处的正极反应式均为O2+4e-+4H+═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
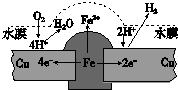 铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )| A、因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀 |
| B、若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小 |
| C、铜极上的反应是2H++2e-═H2↑,O2+4e-+4H+═2H2O |
| D、在金属表面涂一层油脂,能防止铁铆钉被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有化学键断裂的过程一定发生化学变化 | ||
| B、氯化钠是一种电解质,电解饱和食盐水可制得金属钠 | ||
C、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| D、SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体 析出 |
蛋白质均发生变性 |
| B | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色 沉淀 |
溶液X中不一定含有SO42- |
| C | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色 沉淀 |
H2SiO3的酸性比H2CO3的酸性强 |
| D | 向浓度均为0.1mol?L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色 沉淀 |
Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序:W>Z>Y>X |
| B、化合物Z2Y2与X2Y反应时,Z2Y2既是氧化剂又是还原剂 |
| C、元素Y的简单气态氢化物的热稳定性比W的弱 |
| D、由X、Y、Z、W四种元素组成的化合物对水的电离平衡一定是促进的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com