
| A、有化学键断裂的过程一定发生化学变化 | ||
| B、氯化钠是一种电解质,电解饱和食盐水可制得金属钠 | ||
C、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| D、SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
| c(CH3COOH) |
| c(H+) |
| c(CH3COO-) |
| K |
| c(CH3COOH) |
| c(H+) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH4与SiH4的稳定性:CH4>SiH4 |
| B、HClO与H2SO4的酸性:HClO>H2SO4 |
| C、1mol HCl(g)的能量比1mol H2(g)和1mol Cl2(g)的能量和高 |
| D、Cl与S的原子半径:Cl>S |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA |
| B、常温下,1L O.1mol/L NH4NO3的溶液中含氮原子数为0.2NA |
| C、室温下,21.Og乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用新制氢氧化铜悬浊液无法鉴别葡萄糖和乙酸 |
| B、乙酸与乙醇可以发生酯化反应,又均可与碳酸氢钠溶液反应 |
| C、硫酸铵、硫酸铜和乙醇均能使蛋白质变性 |
| D、二氯甲烷不存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
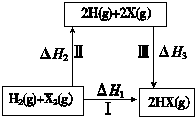 关于如图所示转化关系(X代表卤素),说法不正确的是( )
关于如图所示转化关系(X代表卤素),说法不正确的是( )| A、2H(g)+2X(g)═2HX(g)△H3<0 |
| B、途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 |
| C、Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
| D、途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L SO3中含有的氧原子数为3NA |
| B、标准状况下,22.4L Cl2与足量的稀NaOH 溶液反应,转移电子总数为2NA |
| C、1mol N5+共有34NA核外电子 |
| D、0.5mol CCl4中含有共价键数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、石油通过分馏可直接得到乙烯 |
| B、乙烯、聚乙烯的最简式均为CH2,二者互为同分异构体 |
| C、可用氢氧化钠溶液来区别乙醇和乙酸 |
| D、乙醇、乙酸和乙酸乙酯都能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com