
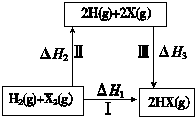
 关于如图所示转化关系(X代表卤素),说法不正确的是( )
关于如图所示转化关系(X代表卤素),说法不正确的是( )| A、2H(g)+2X(g)═2HX(g)△H3<0 |
| B、途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3 |
| C、Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次增多 |
| D、途径Ⅰ生成HCl放出的热量比生成HBr的多,说明HCl比HBr稳定 |


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g?L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Z与Y两种元素组成的化合物中,阴、阳离子个数比为1:1或1:2 |
| B、Y、Z、W元素形成的简单离子具有相同电子层结构,其离子半径依次增大 |
| C、Z、R元素的氧化物的水化物之间相互反应生成的盐溶液呈中性、碱性或酸性 |
| D、Y、R元素分别与X元素形成的化合物的沸点:XmY<XmR |
查看答案和解析>>
科目:高中化学 来源: 题型:
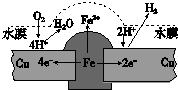 铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )
铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如图.下列说法不正确的是( )| A、因铁的金属性比铜强,所以铁铆钉被氧化而腐蚀 |
| B、若水膜中溶解了SO2,则铁铆钉腐蚀的速率变小 |
| C、铜极上的反应是2H++2e-═H2↑,O2+4e-+4H+═2H2O |
| D、在金属表面涂一层油脂,能防止铁铆钉被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有化学键断裂的过程一定发生化学变化 | ||
| B、氯化钠是一种电解质,电解饱和食盐水可制得金属钠 | ||
C、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| D、SiO2是酸性氧化物,能与强碱溶液反应,但不与任何酸反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、服用铬含量超标的药用胶囊会对人对健康造成危害 |
| B、食用一定量的油脂能促进人体对某些维生素的吸收 |
| C、CH4和Cl2在光照条件下反应的产物最多可能有四种 |
| D、无论乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体 析出 |
蛋白质均发生变性 |
| B | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色 沉淀 |
溶液X中不一定含有SO42- |
| C | 向一定浓度的Na2SiO3溶液中通入适量CO2气体 | 出现白色 沉淀 |
H2SiO3的酸性比H2CO3的酸性强 |
| D | 向浓度均为0.1mol?L-1 NaCl和NaI混合溶液中滴加少量AgNO3溶液 | 出现黄色 沉淀 |
Ksp(AgCl)>Ksp(AgI) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用植物油的加成反应可以制得人造黄油 |
| B、75%的酒精可使蛋白质变性从而起到消毒作用 |
| C、纤维素在人体内可水解成葡萄糖,供人体组织的营养需要 |
D、可用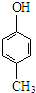 和HCHO为原料合成 和HCHO为原料合成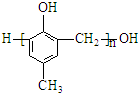 |
查看答案和解析>>
科目:高中化学 来源: 题型:

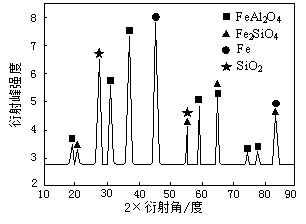
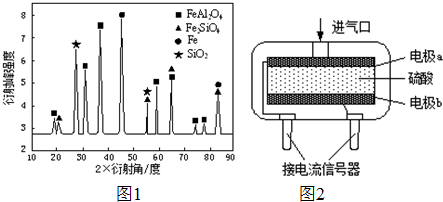
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com