
【题目】碳酸镁晶体是一种新型吸波隐形材料中的增强剂。
实验一:合成碳酸镁晶体的步骤:
①配制一定浓度的MgSO4溶液和NH4HCO3溶液;
②量取一定量的NH4 HCO3溶液于容器中,搅拌并逐滴加入MgSO4溶液,控制温度50℃,反应一段时间;
③用氨水调节溶液pH至9.5,放置一段时间后,过滤、洗涤、干燥得碳酸镁晶体产品。
称取3.000gMgSO4样品配制250mL溶液流程如图所示:
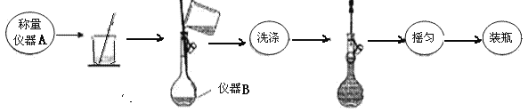
回答下列问题:
(1)写出实验仪器名称:A_____;B_____。配制溶液过程中定容后的“摇匀”的实验操作为______。
(2)检验碳酸镁晶体是否洗干净的方法是_________。
实验二:测定产品MgCO3·nH2O中的n值(仪器和药品如图所示):
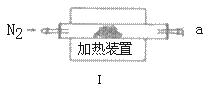
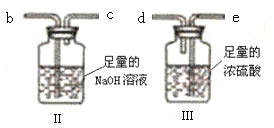
(3)实验二装置的连接顺序为_____(按气流方向,用接口字母abcde表示),其中Ⅱ装置的作用是_____。
(4)加热前先通入N2排尽装置Ⅰ中的空气,然后称取装置Ⅱ、Ⅲ的初始质量。进行加热时还需通入N2的作用是______。
(5)若要准确测定n值,至少需要下列所给数据中的_____(填选项字母),写出相应1种组合情景下,求算n值的数学表达式:n=______。
a.装置Ⅰ反应前后质量差m1 b.装置Ⅱ反应前后质量差m2 c.装置Ⅲ反应前后质量差m3
【答案】电子天平 250mL容量瓶 把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀 取最后一次洗涤液少许于试管,加入稀盐酸酸化,再加入几滴氯化钡溶液,若不再产生白色沉淀,则说明沉淀已洗干净 a→e、d→b 吸收CO2以便测定样品中碳元素的含量 将分解生成的气体全部带入装置B或C中,使其完全吸收,并防止倒吸 a、b(或a、c或b、c) n=22(m1—m2)/9m2[或n=22m3/9(m1—m3)或n=22m3/9m2]
【解析】
(1)实验仪器A为称量MgSO4的仪器,所以名称为电子天平;仪器B是配置250mL溶液的仪器,所以B为250moL容量瓶。配制溶液过程中定容后的“摇匀”的实验操作为把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀。
答案:电子天平;250mL容量瓶;把容量瓶瓶塞塞紧,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶上下颠倒摇动多次,使溶液混合均匀。
(2)检验碳酸镁晶须是否洗干净的方法是检验反应物的硫酸根是否存在,如果不存在硫酸根,说明沉淀洗涤干净,具体的方法是:取最后一次洗涤液少许于试管,加入稀盐酸酸化,再加入几滴氯化钡溶液,若不产生白色沉淀,则说明沉淀已洗干净。
(3)高温加热MgCO3·nH2O,产生CO2和H2O;反应方程式为:MgCO3·nH2O![]() CO2和H2O,通过测定CO2和H2O的质量,就可以测出 MgCO3·nH2O结晶水的含量,装置D用于吸收测量H2O,装置C用于吸收测量CO2。所以正确的连接顺序为a→e、d→b。使MgCO3·nH2O完全分解需要高温,所以装置B的作用为冷却分解产生的高温气体。装置C用于吸收测量CO2。
CO2和H2O,通过测定CO2和H2O的质量,就可以测出 MgCO3·nH2O结晶水的含量,装置D用于吸收测量H2O,装置C用于吸收测量CO2。所以正确的连接顺序为a→e、d→b。使MgCO3·nH2O完全分解需要高温,所以装置B的作用为冷却分解产生的高温气体。装置C用于吸收测量CO2。
答案:a→e、d→b ;吸收CO2以便测定样品中碳元素的含量 。
(4)通入N2,一方面为了将分解生成的气体全部带入装置C或D中,使其完全吸收;另一方面,在反应结束后,高温气体冷却,体积收缩,装置C和D的液体可能会发生倒吸,反应结束后继续通入N2可以防止倒吸。将分解生成的气体全部带入装置B或C中,使其完全吸收,并防止倒吸
(5)B装置中无残留物表明气体全部进入装置C和D,如想准确测定![]() 值,则需要知道三个质量差中的两个。所以要知道a、b(或a、c或b、c)。计算过程如下:
值,则需要知道三个质量差中的两个。所以要知道a、b(或a、c或b、c)。计算过程如下:
MgCO3·nH2O![]() CO2+ nH2O + MgO 固体质量减轻
CO2+ nH2O + MgO 固体质量减轻
100+18n 44 18n 44+18n
m2 m3 m1
由此44/18n=m2/m3,解得n=22m3/9m2,又有m1=m2+m3,通过转换,可以得到n=22(m1—m2)/9m2[或n=22m3/9(m1—m3)或n=22m3/9m2]。
答案:a、b(或a、c或b、c) ; n=22(m1—m2)/9m2[或n=22m3/9(m1—m3)或n=22m3/9m2]。


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
【题目】根据下图,回答问题。
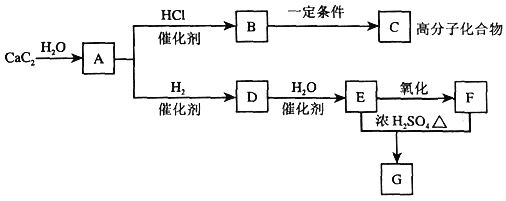
(1)B中所含官能团的名称是:_______。
(2)反应B→C的化学方程式是________;反应D→E的化学方程式是_______。
(3)B→C的反应类型属于______。
(4)写出实验室制取A的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
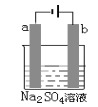
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示装置中,甲池的总反应式为2CH3OH+ 3O2+ 4KOH=2K2CO3+ 6H2O。试回答:
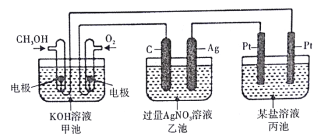
(1)图中甲池的装置是_________(填“原电池”或“电解池”),乙池中石墨电极是________极。
(2)写出通入CH3OH的电极的电极反应式:________________
(3)乙池中总反应的化学方程式为___________________
(4)当乙池中Ag极的质量增加5.40g时,甲池中理论上消耗O2________mL(标准状况);此时丙池某电极上析出1.60g某金属,则丙池中的盐溶液可能是________(填字母)
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解是一种非常强有力的促进氧化还原反应的手段,许多很难进行的氧化还原反应,都可以通过电解来实现。
(1)工业上常以石墨做电极,电解NaCl水溶液时,阴极区产物有____,其溶液可用于吸收工业尾气中的SO2,写出反应的化学方程式_____。
(2)电解NaCl水溶液时,用盐酸控制阳极区溶液的pH在2~3,用平衡移动原理解释盐酸的作用_____。离子液体是一种室温熔融盐,为非水体系。由有机阳离子、Al2Cl7-和AlCl4-组成的离子液体作电解液时,可在钢制品上发生电镀,有铝产生。
(3)铝原子的核外电子排布式是____,其中有____种不同能级的电子。
(4)为测定镀层厚度,用NaOH溶液溶解钢制品表面的铝镀层,当所得还原产物为6g时,转移电子的物质的量为___mol。
(5)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有____(填编号)。
a.KClO3 b.Mg c.MnO2 d.KCl
取少量铝热反应所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,不能说明固体混合物中无Fe2O3,理由是________(用离子方程式说明)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热(不与外界发生热交换)的恒容容器中,发生反应:2A(g)+B(s) ![]() C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
C(g)+D(g),下列描述中能表明反应已达到平衡状态的有( )个
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤C(g)的物质的量浓度不变
⑥容器内A、C、D三种气体的浓度之比为2:1:1 ⑦某时刻v(A)=2v(C)且不等于零
⑧单位时间内生成n mol D,同时生成2n mol A
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 实验结论 |
A |
| 装置气密性良好 |
B | 将氧化铁加入到足量的HI溶液中,充分溶解后,滴加四氯化碳,震荡静置,下层呈紫红色。 | I2氧化性强与Fe3+ |
C | 往氢氧化铜沉淀中分别滴加盐酸和氨水,沉淀皆溶解 | 氢氧化铜为两性氢氧化物 |
D | 将SO2通入Na2CO3溶液中生成的气体,通入澄清石灰水中有浑浊 | 说明酸性:H2SO3﹥H2CO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组,将剪下的一块镀锌铁放入试剂瓶中,并滴入少量食盐水将其浸湿,再加数滴酚酞溶液,按图装置进行实验,数分钟后观察,下列现象不可能出现的是( )

A. B中导气管里形成一段水柱
B. B中导气管中产生气泡
C. 金属片剪口处溶液变红
D. 锌被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法中,正确的是
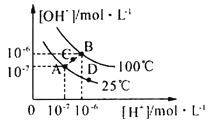
A.图中A、B、D三点处Kw的大小关系:B>A>D
B.25℃时,向pH=1的稀硫酸中逐滴加入pH=8的稀氨水,溶液中c(NH4+)/c(NH3·H2O)的值逐渐减小
C.在25℃时,保持温度不变,在水中加人适量NH4Cl固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在Na+、Fe3+、Cl-、SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com