
【题目】在标准状况下①6.72LCH4②3.01×1023个HCl分子③13.6gH2S④0.2molNH3,下列对这四种气体的关系从大到小表达正确的是( )
a.体积②>③>①>④ b.密度②>③>④>① c.质量②>③>①>④ d.氢原子个数①>③>④>②
A. abc B. bcd C. abcd D. acd
【答案】D
【解析】
试题①6.72L CH4物质的量为![]() =0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol,③13.6g H2S 的物质的量为
=0.3mol,②3.01×1023个HCl分子的物质的量为0.5mol,③13.6g H2S 的物质的量为![]() =0.4mol,④0.2mol NH3。a、相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>③>①>④,故a正确;b、各物质的摩尔质量分别为①CH4为16g/mol②HCl为36.5g/mol ③H2S 为34g/mol④NH3为17g/mol,相同条件下,密度之比等于摩尔质量之比,所以密度②>③>④>①,故b正确;c、各物质的质量分别为①CH4为0.3mol×16g/mol=4.8g②HCl为0.5mol×36.5g/mol="33.25g" ③H2S 13.6g④NH3为0.2mol×17g/mol=3.4g,所以质量②>③>①>④,故c正确;d、各物质中H原子的物质的量分别为①CH4为0.3mol×4=1.2mol②HCl为0.5mol③H2S 0.4mol×2=0.8mol④NH3为0.2mol×3=0.6mol,所以氢原子个数①>③>④>②,故d正确。故选C。
=0.4mol,④0.2mol NH3。a、相同条件下,气体的体积之比等于物质的量之比,所以体积体积②>③>①>④,故a正确;b、各物质的摩尔质量分别为①CH4为16g/mol②HCl为36.5g/mol ③H2S 为34g/mol④NH3为17g/mol,相同条件下,密度之比等于摩尔质量之比,所以密度②>③>④>①,故b正确;c、各物质的质量分别为①CH4为0.3mol×16g/mol=4.8g②HCl为0.5mol×36.5g/mol="33.25g" ③H2S 13.6g④NH3为0.2mol×17g/mol=3.4g,所以质量②>③>①>④,故c正确;d、各物质中H原子的物质的量分别为①CH4为0.3mol×4=1.2mol②HCl为0.5mol③H2S 0.4mol×2=0.8mol④NH3为0.2mol×3=0.6mol,所以氢原子个数①>③>④>②,故d正确。故选C。


科目:高中化学 来源: 题型:
【题目】以节能减排为基础的低碳经济是保持社会可持续发展的战略举措。下列做法违背发展低碳经济的是
A.发展氢能和太阳能
B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学
D.尽量用纯液态有机物代替水作溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等电子原理:原子数相同、最外层电子总数相同的分子互称为等电子体。等电子体的结构、物理性质均相似。
(1)根据以上原理,仅由第二周期元素组成的共价化合物分子中,互为等电子体的是__________和__________;________和________。
(2)此后,等电子原理又有发展。例如:由短周期元素组成的粒子,只要其原子总数相同,各原子最外层电子数之和相同,也可互称为等电子体,它们也具有相似的结构特征。在短周期元素组成的物质中,与NO![]() 互为等电子体的分子有:_________(写出一种即可)。
互为等电子体的分子有:_________(写出一种即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在______ molAl2(SO4)3中含0.3 mol SO42–,含Al3+约_______________个。
(2)同温同压下,相同质量的SO2气体和SO3气体,其分子数之比为_________,密度之比为_________。
(3)质量同为46 g的两种气体,NO2和N2O4,物质的量之比为________,二者所含O原子个数之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2014年多位演艺明星因涉毒锒铛入狱,演出一部阵容豪华的“监狱风云”。吸毒祸害之大,胜于洪水猛兽。下列物质中不属于毒品的是( )
A. 冰毒 B. 吗啡
C. 摇头丸 D. 阿司匹林
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石油产品A(C3H6)为主要原料,合成具有广泛用途的有机玻璃PMMA。流程如下(部分产物和条件省略)
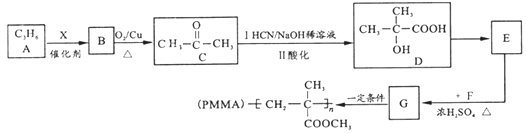
试回答下列问题:
(1)B的名称________;X试剂为_______(化学式);D中官能团名称_________。
(2)E→G的化学方程式为________________________________________,反应类型是_________。
(3)T是G的同分异构体,1molT与足量新制Cu(OH)2悬浊液反应最多生成2molCu2O沉淀,T的结构有________种(不含立体结构)。
(4)若高分子化合物PMMA的相对分子质量为1.5×106,其聚合度为_______。
(5)参照上述流程,以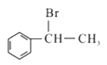 为原料合成
为原料合成 (其它原料自选)。设计合成路线:________________________。
(其它原料自选)。设计合成路线:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄红色液体二氯化二硫可以作为贵稀金属的萃取剂,由硫与氯气再50℃~60℃直接化合而成。装置图如下:

(1)二氯化二硫遇水会反应,生成硫、二氧化硫和刺鼻的酸雾,其化学方程式为______。
(2)A装置中所盛试剂为__________。
(3)操作过程中:
①先通入N2,理由是_________________。
②通入少量Cl2后,装置B采用________(填“水浴”或“油浴”)加热1h。
③停止加热,加大通入氯气量,维持16h。制备二氯化二硫为______(填“放热”或“吸热”)反应。
(4)二氯化二硫的电子式为______________。
(5)装置C的作用是__________,同时制得有价值的工业产品为___________。
(6)为了得到更纯净的二硫化二氯,需要在装置B、C之间安装干燥管,其内盛试剂为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
磷及其化合物是生活生产中重要的组成部分,以下是一些常见的磷的化合物:
(1)与磷同主族、比磷多一个周期的元素基态原子的价层电子排布为___________.
(2)磷与同周期相邻的两种元素的第一电离能由大到小的顺序为__________。(用元素符号表示)。
(3)亚磷酸(H3PO3)是一种常见的无机酸,其与过量的NaOH溶液反应生成Na2HPO3,请画出亚磷酸的分子结构_______。亚磷酸可作还原剂将Cu2+还原为单质,得到的电子填充到________轨道。
(4)己知PBr5晶体中存在PBr4+,和Br-两种离子,则PBr4+,中心P原子杂化类型为___,该离子的几何构型为______。而PCl5晶体中存在PCl4+和另一种阴离子,该阴离子配位数为6,请写出该离子的化学式:______。PBr5晶体中不能形成与PCl5晶体一样的阴离子的原因可能是:_________。
(5)铝和白磷在一定条件下可以制备磷化铝(AlP),磷化铝晶胞的结构如图,可以将其看做Si晶体的“广义等电子体”,可做半导体材料.
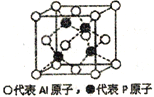
①根据“广义等电子原理”,下列物质中,可能是半导体的有____________.
A. SiC B.CaO2 C. GaAs D.Si3N4 E.BN
②磷化铝中,Al原子的配位数为_______,若该晶胞密度为dg/cm3,用NA表示阿伏伽德罗常数,则该晶体的边长为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是
A. 2 mol水的摩尔质量和1 mol水的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 标准状况下,22.4 L一氧化碳中氧原子数和16 g二氧化硫中氧原子数
D. 2 mol·L-1H2SO4溶液中的H+个数与1 mol·L-1HCl溶液中的H+个数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com