
| A. | 该溶液中离子浓度关系为:c (Na+)>c(HCO3-)>c (OH-)>c(H+) | |
| B. | 25℃时,加水稀释后,$\frac{c(O{H}^{-})}{c({H}^{+})}$变小 | |
| C. | 温度升高,c(OH-)×c(H+)不变(忽略体积变化) | |
| D. | 溶液中c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
分析 A.碳酸氢钠溶液中碳酸氢根离子水解程度大于碳酸氢根离子电离程度,溶液显碱性;
B.加水稀释促进电离,氢氧根离子浓度减小,一定温度下溶液中离子积常数不变,氢离子浓度增大;
C.升温促进水的电离,离子积常数增大;
D.溶液中存在物料守恒分析,n(Na)=n(C).
解答 解:A.碳酸氢钠溶液中碳酸氢根离子水解程度大于碳酸氢根离子电离程度,溶液显碱性,溶液中离子浓度关系为:c (Na+)>c(HCO3-)>c (OH-)>c(H+),故A正确;
B.25℃时,碳酸氢钠溶液加水稀释后,氢氧根离子浓度减小,氢离子浓度增大,所以$\frac{c(O{H}^{-})}{c({H}^{+})}$比值减小,故B正确;
C.升温促进水的电离,离子积常数c(OH-)×c(H+)增大,故C错误;
D.0.10mol•L-1 NaHCO3溶液中存在物料守恒c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故D正确;
故选C.
点评 本题考查了盐类水解原理、水的离子积常数、电解质溶液中物料守恒的分析应用,注意影响水电离平衡的因素,题目难度中等.


科目:高中化学 来源: 题型:多选题
 在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )
在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )| A. | 该化学反应在3min时达到平衡状态 | |
| B. | 保持其他条件不变,降低温度,平衡时c(CH3OH)=0.85 mol•L-1,则该反应的△H<0 | |
| C. | 相同温度下,起始时向上述容器中充入0.5molCO2、1.5molH2,平衡时CO2的转化率小于75% | |
| D. | 12min时,向上述容器中再充入0.25molCO2、0.25molH2O(g),此时反应将向逆反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
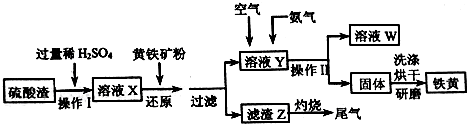
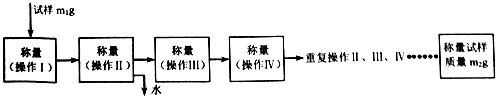
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中含有OH- | B. | 与氯化铵溶液反应放出氨气 | ||
| C. | 与金属铝反应放出氢气 | D. | 滴入甲基橙试液后,溶液呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:3 | B. | 3:1 | C. | 1:24 | D. | 24:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
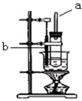 实验室制取硝基苯的装置如图所示.
实验室制取硝基苯的装置如图所示.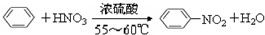 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径/(10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | -- |
| 最低负价 | -- | -1 | -- | --- | -3 | -2 | |
| A. | 由元素X和Q组成的化合物不可能含有共价键 | |
| B. | X、Z、R的最高价氧化物对应水化物可彼此反应 | |
| C. | Y-半径比Q2-半径大 | |
| D. | M(OH)2的碱性比XOH的碱性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤、石油、天然气均为化石燃料,它们属于可再生资源 | |
| B. | 生物质能来源于植物及其加工产品所贮存的能量 | |
| C. | 氢气的燃烧产物是水,不会污染环境,是理想的清洁燃料 | |
| D. | 大自然利用太阳能最成功的是植物的光合作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com