
 ;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
;另一种没有支链且能被氧化成醛,写出它与乙酸发生酯化反应的方程式CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O.
 .
. 和CH3COOH(写结构简式).
和CH3COOH(写结构简式). 分析 Ⅰ.①1mol有机物可与2mol溴单质发生加成反应,则含2个碳碳双键或1个碳碳三键;
②核磁共振氢谱只有一个吸收峰,则分子中只有1种位置的H;
③能发生银镜反应,则含-CHO;
Ⅱ.分子式为C4H10O,属于醇,可看作丁烷中H被-OH取代,丁基有4种;与-OH相连的C上不含H,则不能被氧化;没有支链且能被氧化成醛,则为1-丁醇,与乙酸发生酯化反应生成酯和水;
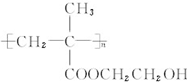
Ⅲ.①由C的结构可知,高分子B为C水解产物;
②A与B发生酯化反应生成C;
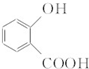
③A中含-COOC-,水解生成邻羟基苯甲酸和乙酸.
解答 解:Ⅰ.①1mol有机物可与2mol溴单质发生加成反应,则含2个碳碳双键或1个碳碳三键,只有乙炔符合,故答案为:B;
②核磁共振氢谱只有一个吸收峰,则分子中只有1种位置的H,只有苯中含1种位置的H,故答案为:A;
③能发生银镜反应,则含-CHO,只有葡萄糖中含-CHO,故答案为:C;
Ⅱ.分子式为C4H10O,属于醇,可看作丁烷中H被-OH取代,丁基有4种,则醇有4种;与-OH相连的C上不含H,则不能被氧化,其结构简式为 ;没有支链且能被氧化成醛,则为1-丁醇,与乙酸发生酯化反应生成酯和水,该反应为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O,
;没有支链且能被氧化成醛,则为1-丁醇,与乙酸发生酯化反应生成酯和水,该反应为CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O,
故答案为:4; ;CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O;
;CH3COOH+CH3CH2CH2CH2OH$?_{△}^{浓硫酸}$CH3COOCH2CH2CH2CH3+H2O;
Ⅲ.①由C的结构可知,高分子B为C水解产物,则B为 ,故答案为:
,故答案为: ;
;
②A与B发生酯化反应生成C,反应类型为酯化反应,也属于取代反应,故答案为:酯化反应;
③A中含-COOC-,水解生成邻羟基苯甲酸和乙酸,结构简式分别为 、CH3COOH,故答案为:
、CH3COOH,故答案为: ;CH3COOH.
;CH3COOH.
点评 本题考查有机物的结构与性质,为高频考点,综合性较强,涉及官能团与性质、同分异构体、有机反应、高分子化合物结构等,题目难度不大.


 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:解答题
 某研究性学习小组设计了一组实验验证元素周期律.非金属性越强,对应的最高价含氧酸的酸性就越强.他设计了如图装置以验证碳、氮、硅元素的非金属性强弱.已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成.
某研究性学习小组设计了一组实验验证元素周期律.非金属性越强,对应的最高价含氧酸的酸性就越强.他设计了如图装置以验证碳、氮、硅元素的非金属性强弱.已知A是强酸,常温下可与铜反应;B是块状固体;打开分液漏斗的活塞后,C中可观察到白色沉淀生成.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.6mol/(L•min) | ||
| C. | v(c)=0.4mol/(L•min) | D. | v(D)=0.45mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 半径(pm) | 30 | 64 | 66 | 91 | 70 | 106 | 110 | 186 | 125 | 232 |
| 主要 化合价 | -1,+1 | -1 | -2 | -4, +4 | -3, +5 | -2,+4,+6 | -4, +4 | +1 | +3 | +1 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定相同 | B. | 一定不同 | C. | 可能不同 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大c(X),X的转化率增大 | B. | 降低温度,Y的转化率增大 | ||
| C. | 减小容器体积,平衡向右移动 | D. | 加入催化剂,Z的产率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M的能量一定低于X的,N的能量一定低于Y的 | |
| B. | 因为该反应为吸热反应,故一定要加热反应才能进行 | |
| C. | 破坏反应物中化学键吸收的能量小于形成生成物中化学键所放出的能量 | |
| D. | M和N的总能量一定低于X和Y的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

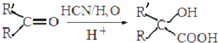
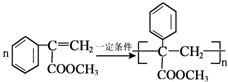
 生成
生成 的反应类型是取代反应.
的反应类型是取代反应. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18gH2O所含的电子数目为9N0 | |
| B. | 0.1 mol/L Na2SO4溶液所含Na+数目为0.2N0 | |
| C. | 1 mol钠完全反应时所失去的电子数为N0 | |
| D. | 标准状况下22.4L O2所含的原子数目为N0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com