
| A、生活中用碱液洗涤铝制饮具 |
| B、用小苏打治疗胃酸过多 |
| C、用漂白粉做公共泳池的消毒剂 |
| D、铁、铜制品应要保持干燥,以防生锈 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 X、Y、Z、W、Q为五种常见化合物,R为常见单质;X、Y、Z、Q的焰色反应均为黄色,常温下W、R均为无色无味气体.其转化关系如图所示(部分反应物、产物及反应条件已略去)
X、Y、Z、W、Q为五种常见化合物,R为常见单质;X、Y、Z、Q的焰色反应均为黄色,常温下W、R均为无色无味气体.其转化关系如图所示(部分反应物、产物及反应条件已略去)查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图1中醋酸电离平衡常数:a点的比b点的小 |
| B、图1中醋酸溶液的pH:b点的比a点的大 |
| C、图2中c点对应的溶液为Fe(OH)3的不饱和溶液 |
| D、由图2可知,欲除去CuSO4溶液中的Fe3+,可向溶液中加入适量CuO,调pH约为4左右 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、弱碱 | B、一元强碱 |
| C、多元强碱 | D、任何强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、电池反应的化学方程式为:2Li+FeS═Li2S+Fe |
| B、负极的电极反应式为:Al-3e-=Al3+ |
| C、Li-Al在电池中作为负极材料,该材料中Li的化合价是+1 |
| D、电池充电时,阴极反应为:Li2S+Fe-2e-═2Li++FeS |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol/L NaClO溶液:Fe2+、K+、I-、Cl- | ||
| B、通入足量CO2后的溶液中:Na+、C6H5O-、CH3COO-、HCO3- | ||
| C、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y元素原子最外层电子数与核外电子总数之比为3:4,M元素原子的最外层电子数与次外层电子数之比为3:4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体,据此回答下列问题:
元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大.已知Y元素原子最外层电子数与核外电子总数之比为3:4,M元素原子的最外层电子数与次外层电子数之比为3:4,且M原子的质子数是Y原子的2倍;N-、Z+、X+的半径逐渐减小;化合物XN在常温下为气体,据此回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
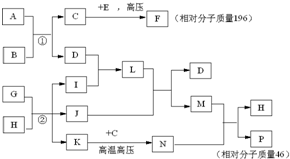 已知C、I、J是常见的气体,A、D是常见的固态非金属单质,E为常见金属,B可用于生产光导纤维,G、H是海水中的主要物质,N是一种盐.在核磁共振氢谱中P有两种峰,F燃烧产生红棕色烟,1molF在真空中完全分解剩余固体的质量是原来的28.6%.试回答下列问题
已知C、I、J是常见的气体,A、D是常见的固态非金属单质,E为常见金属,B可用于生产光导纤维,G、H是海水中的主要物质,N是一种盐.在核磁共振氢谱中P有两种峰,F燃烧产生红棕色烟,1molF在真空中完全分解剩余固体的质量是原来的28.6%.试回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com