
I.光伏组件采用高效率单晶硅或多晶硅光伏电池、高透光率钢化玻璃、抗腐蚀铝合多边框等材料,使用先进的真空层压工艺及脉冲焊接工艺制造。
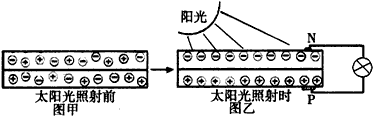
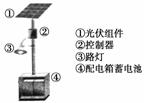 (1)下图是太阳能电池板经太阳光照射前后内部电子的变化情况,图乙中灯泡变亮,其中____(填写“N”或“P”)是正极。
(1)下图是太阳能电池板经太阳光照射前后内部电子的变化情况,图乙中灯泡变亮,其中____(填写“N”或“P”)是正极。
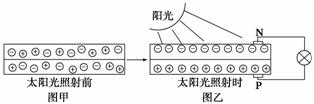
![]() (2)右上图是一个太阳能路灯,图中的④是蓄电池。镍氢电池就是这样一种与太阳能电池配套使用的蓄电池,白天用于充电,夜间供电。这种蓄电池容量大,充电放电循环寿命也较长。该蓄电池的总反应为Ni(OH)2 NiOOH+1/2H2↑。镍氢电池的电解液采用30%的KOH溶液,白天充电反应时的阳极反应式为 ,夜间放电时,负极附近溶液的pH________(填“增大”、“减小”或“不变”)。
(2)右上图是一个太阳能路灯,图中的④是蓄电池。镍氢电池就是这样一种与太阳能电池配套使用的蓄电池,白天用于充电,夜间供电。这种蓄电池容量大,充电放电循环寿命也较长。该蓄电池的总反应为Ni(OH)2 NiOOH+1/2H2↑。镍氢电池的电解液采用30%的KOH溶液,白天充电反应时的阳极反应式为 ,夜间放电时,负极附近溶液的pH________(填“增大”、“减小”或“不变”)。
 II.X、Y、Z、Q、R5种短周期元素原子序数依次增大。化合物甲由X、Z、Q3种元素组成,常温下,0.1mol·L-l甲溶液的pH =13。工业上常用电解QR饱和溶液生产甲
II.X、Y、Z、Q、R5种短周期元素原子序数依次增大。化合物甲由X、Z、Q3种元素组成,常温下,0.1mol·L-l甲溶液的pH =13。工业上常用电解QR饱和溶液生产甲
(3)Q的原子结构示意图为
(4)常温下将R的单质通人甲溶液中,发生反应的离子方程式为
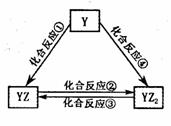
(5)若Y元素的单质能发生如右图所示转化,则Y元素是 。
已知:298K时,反应②生成1mol YZ2(g)时放出热量283.O kJ·mol-1,
反应④生成1mol YZ2(g)时放出热量393.5 kJ·mol-1,反应③的热化学方程式为
。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
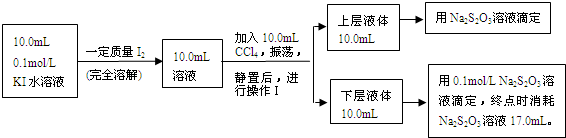
| c[I2(CCl4)] |
| c[I2(H2O)] |
| 0.049mol/L |
| 0.001mol/L×0.051mol/L |
| 0.049mol/L |
| 0.001mol/L×0.051mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
铜单质及其化合物在很多领域有重要的用途,如金属铜用来制造电线电缆,五水硫酸铜可用作杀菌剂。
(1)Cu位于元素周期表第I B族。Cu2+的核外电子排布式为 。
(2)右图是铜的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 。
(3)胆矾CuSO4·5H2O可写成[Cu(H2O)4]SO4 H2O,其结构示意图如下:

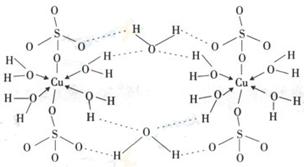
下列说法正确的是 (填字母)。
A.在上述结构示意图中,所有氧原子都采用sp3杂化
B.在上述结构示意图中,存在配位键、共价键和离子键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(4)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH2)2]2+配离子。已知NF3与NH3的空间构型都是三角锥形,单NF3不易与Cu2+形成配离子,其原因是 。
(5)Cu2O的熔点比Cu2S的 (填“高”或“低”),请解释原因 。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:填空题
 NiOOH+1/2H2↑。
NiOOH+1/2H2↑。 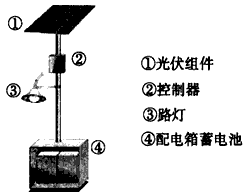
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com