
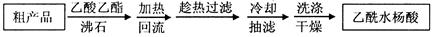
| A.称取0.300 g样品。 |
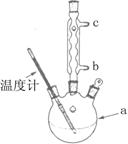
| B.将样品与25 mL 4 mol·L-lNaOH溶液在三颈烧瓶中混合,水浴加热回流l小时后停止加热(发生的反应为:C6H5CH2Cl+NaOH→C6H5CH2OH+ NaCl)。 |
| C.在三颈烧瓶中加入50 mL 2 mol·L-l HNO3,混合均匀。 |
| D.将三颈烧瓶中溶液全部转移到100 mL容量瓶中,加水定容。 |
 (2分)
(2分) 。
。

科目:高中化学 来源:不详 题型:单选题




 ( )
( )| A.纸层析法中滤纸所吸附的水作固定相,不与水混溶的有机溶剂作流动相 |
| B.分液操作时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出 |
| C.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| D.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B.眼睛里溅进了少量酸或碱溶液,要立即用大量水冲洗,边洗边眨眼睛 |
| C.不慎洒出的酒精在桌上燃烧起来,应立即用大量水扑灭 |
| D.将含硫酸的废液倒入水槽,用水冲入下水道 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.燃烧法测定有机物组成时先用碱石灰测CO2质量,再用浓H2SO4测H2O质量 |
| B.制硝基苯需要配制混合酸,应先加浓硝酸再加浓硫酸 |
| C.检验淀粉在稀硫酸作用下是否发生水解,应在水解液中先加入NaOH溶液中和后再加入银氨溶液共热 |
| D.检验丙烯醛(CH2=CH—CHO)中的官能团时,应先用新制Cu(OH)2试剂检验醛基再用KMnO4溶液检验碳碳双键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将一块未擦去氧化膜的铝片放入适量0.5mol·L-1CuSO4溶液中,铝片表面无明显现象 |
| B.向其中一支试管中加入1mL乙醇,向另一支试管中加入约1.5g苯酚。再向上述两支试管中各加一小块吸干煤油的金属钠,比较乙醇和苯酚中羟基上氢原子的活泼性 |
| C.用新制氢氧化铜可以检验牙膏中是否含有甘油,新制氢氧化铜与甘油反应生成绛蓝色溶液 |
| D.用稀KMnO4酸性溶液可以检验火柴头燃烧时是否产生了二氧化硫气体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用倾析法分离时,将烧杯中的上层清液用玻璃棒引流到另一容器内,即可使沉淀与清液分离 |
| B.洗涤沉淀时,应在过滤器中加入洗涤液浸没沉淀,过滤,并重复2到3次 |
| C.抽滤完毕,应先拆下连接抽气泵和吸滤瓶的橡胶管,再关闭水龙头,最后将滤液从吸滤瓶支管口倒出 |
| D.用移液管取液后,将移液管垂直放入稍倾斜的容器中,并使管尖与容器内壁接触,松开食指使溶液全部流出,数秒后,取出移液管 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用药匙取用粉末状或小颗粒状固体 | B.用胶头滴管滴加少量液体 |
| C.给盛有2/3体积液体的试管加热 | D.倾倒液体时试剂瓶标签面向手心 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com