
【题目】CuCl是应用广泛的有机合成催化剂,可从黄铜矿(主要成分为CuFeS2)中制取。
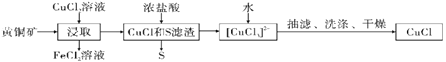
已知:CuCl是一种白色粉末,微溶于水,难溶于乙醇,在空气中易被氧化,在水溶液中存在平衡:CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
[CuCl3]2-(aq)(无色溶液),下列叙述错误的是( )
A.浸取阶段,参加反应的CuFeS2和CuCl2的物质的量之比为3:l
B.浸取所得到的FeCl2溶液,可用来腐蚀覆在绝缘板上的铜箔制造印刷电路板
C.加水有利于CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl
[CuCl3]2-(aq)平衡逆向移动,析出CuCl
D.为提高产率和纯度,可采用乙醇洗涤、真空干燥
【答案】AB
【解析】
黄铜矿和氯化铜反应生成氯化亚铜、氯化亚铁和硫单质,CuCl和盐酸反应生成[CuCl3]2-,加水稀释利用平衡移动原理CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq),平衡逆向移动,生成氯化亚铜。
[CuCl3]2-(aq),平衡逆向移动,生成氯化亚铜。
A. 浸取中的主要反应为CuFeS2+3CuCl2= 4CuCl+FeCl2+2S,参加反应的CuFeS2和CuCl2的物质的量之比为1:3,A项错误;
B. 浸取所得到的FeCl2溶液和铜不反应,B项错误;
C. 加水,反应物浓度减小更多,CuCl(s)+2Cl-(aq)![]() [CuCl3]2-(aq)平衡逆向移动,析出CuCl,C项正确;
[CuCl3]2-(aq)平衡逆向移动,析出CuCl,C项正确;
D. 因CuCl微溶于水,难溶于乙醇,在空气中易被氧化,为提高产率和纯度,因此采用乙醇洗涤、真空干燥CuCl,D项正确;
答案选AB。


科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是
A.过量的铁粉溶于稀硝酸:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O
C.用惰性电极电解MgCl2溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
D.室温下,氯化铵溶液pH<7的原因:NH4++H2O=NH3·H2O+H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物I(C11H12O3)是制备液晶材料的中间体之一,其分子中含有醛基和酯基,I可以用E和H在一定条件下合成:
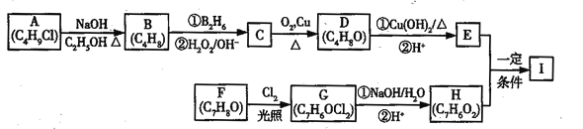
已知以下信息:
①A的核磁共振氢谱表明其只有一种化学环境的氢;
②R﹣CH=CH2![]() R﹣CH2CH2OH;
R﹣CH2CH2OH;
③化合物F苯环上的一氯代物只有两种;
④通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
回答下列问题:
(1)A的化学名称为_______________________________;
(2)D的结构简式为_______________________________;
(3)E中的官能团名称为___________________________;
(4)F生成G的化学方程式为__________________________,该反应类型为______________;
(5)I的结构简式为_________________________________。
(6)I的同系物J比I相对分子质量小14,J的同分异构体中能同时满足如下条件:①苯环上只有两个取代基,②既能发生银镜反应,又能与饱和NaHCO3溶液反应放出CO2,共有____种(不考虑立体异构)。J的一个同分异构体发生银镜反应并酸化后核磁共振氢谱为三组峰,且峰面积比为2:2:1,写出J的这种同分异构体的结构简式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定。
(1)下列仪器中,与该滴定实验无关的为______。
A 胶头滴管 B 量筒(10ml) C 锥形瓶 D 滴定管夹
(2)量取一定体积的白醋所用的仪器_______(填“酸式”或“碱式”)滴定管. 实验中应选用______作指示剂。
(3)滴定过程中进行如下操作,分别指出该项操作对滴定结果的影响(填“偏高”、“偏低”或“无影响”)
Ⅰ滴定前未用标准液润洗碱式滴定管______;
Ⅱ滴定结束时俯视滴定管刻度______
Ⅲ 盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失______
(4)在滴定过程中,当c(CH3COOˉ)< c(Na+)时,则混合溶液呈____(填序号)。
A 酸性 B 碱性 C 中性 D 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
2CO2(g)+N2(g) △H=-746.8kJ·mol-1,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是
A. 降低温度 B. 增大压强
C. 升高温度同时充入N2 D. 及时将CO2和N2从反应体系中移走
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,0.1mol·L-1的某二元酸H2A溶液中,逐渐加入NaOH溶液,可能存在的含A粒子的物质的量分数随pH变化的关系如图所示,下列说法正确的是( )
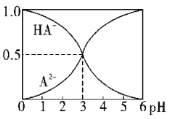
A.H2A的电离方程式:H2A![]() H++HA-
H++HA-
B.pH=5时,在NaHA和Na2A的混合溶液中:c(HA-):c(A2-)=1:100
C.等物质的量浓度的NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c(Na+)>c(A2-)>c(HA-)
D.Na2A溶液必存在c(OH-)=c(H+)+c(HA-)+2c(H2A),各粒子浓度均大于0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某电动汽车配载一种可充放电的锂离子电池,放电时电池总反应为:Li1﹣xCoO2+LixC6═LiCoO2+C6(x<1),下列关于该电池的说法不正确的是( )
A.放电时,Li+在电解质中由负极向正极迁移
B.放电时,负极的电极反应式为LixC6﹣xe﹣═xLi++C6
C.充电时,若转移1mole﹣,石墨(C6)电极将增重7xg
D.充电时,阳极的电极反应式为LiCoO2﹣xe﹣═Li1﹣xCoO2+xLi+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M的结构简式为:有关M的下列叙述中正确的是( )
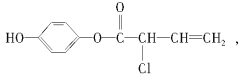
A.可与H2反应,1 mol M最多消耗5 mol H2
B.可与浓溴水反应,1 mol M最多消耗4 mol Br2
C.可与NaOH溶液反应,1 mol M最多消耗4 mol NaOH
D.M不能使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某活动小组利用废铁屑(含少量S等元素)为原料制备硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O],设计如图所示装置(夹持仪器略去)。
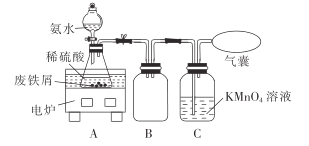
称取一定量的废铁屑于锥形瓶中,加入适量的稀硫酸,在通风橱中置于50~60°C热水浴中加热.充分反应。待锥形瓶中溶液冷却至室温后加入氨水,使其反应完全,制得浅绿色悬浊液。
(1)在实验中选择50~60° C热水浴的原因是___________
(2)装置B的作用是______________;KMnO4溶液的作用是______________。
(3)若要确保获得浅绿色悬浊液,下列不符合实验要求的是_________(填字母)。
a.保持铁屑过量 b. 控制溶液呈强碱性 c.将稀硫酸改为浓硫酸
(4)检验制得的(NH4)2SO4·FeSO4·6H2O中是否含有Fe3+的方法:将硫酸亚铁铵晶体用加热煮沸过的蒸馏水溶解,然后滴加_______(填化学式)。
(5)产品中杂质Fe3+的定量
①配制Fe3+浓度为0.1 mg/mL的标准溶液100 mL。称取______ (精确到0.1)mg高纯度的硫酸铁铵[(NH4)Fe(SO4)2·12H2O],加入20.00 mL经处理的去离子水。振荡溶解后,加入2 mol·L-1HBr溶液1mL和1mol·L-1KSCN溶液0.5mL,加水配成100mL溶液。
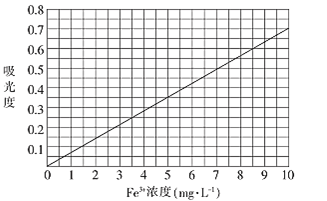
②将上述溶液稀释成浓度分别为0.2、1.0、3.0、5.0、7.0、10.0(单位:mg·L-1)的溶液。分别测定不同浓度溶液对光的吸收程度(吸光度),并将测定结果绘制成如图所示曲线。取硫酸亚铁铵产品,按步骤①配得产品硫酸亚铁铵溶液10mL,稀释至100mL,然后测定稀释后溶液的吸光度,两次测得的吸光度分别为0.590、0.610,则该兴趣小组所配产品硫酸亚铁铵溶液中所含Fe3+浓度为_______mg·L-1。
(6)称取mg产品,将产品用加热煮沸的蒸馏水溶解,配成250mL溶液,取出100mL放入锥形瓶中,用cmol·L-1KMnO4溶液滴定,消耗KMnO4溶液VmL,则硫酸亚铁铵晶体的纯度为_____ (用含c、V 、m的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com