
【题目】下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )。

A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. Y的氢化物的沸点比H2O的沸点高
D. Y元素的非金属性比W元素的非金属性强
 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是 ( )
A.摩尔是表示物质量的单位,每摩尔物质含有6.02×1023个分子
B.1mol氧的质量为16
C.0.5molHe约含有6.02×1023个电子
D.2H既可表示2个氢原子又可表示2mol氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将甲针筒内20mLH2S推入含有10 mLSO2的乙针筒内,一段时间后,对乙针筒内现象描述错误的是(气体在同温同压下测定)( )
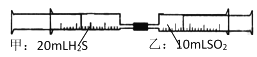
A. 有淡黄色固体生成
B. 有无色液体生成
C. 气体体积缩小
D. 最终约余15mL气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的叙述中,不正确的是
A、金刚石网状结构中,由共价键形成的碳原子环其中最小环有6个碳原子
B、在氯化钠的晶体中,每个Na+或Cl-的周围都紧邻6个Cl-或Na+
C、在氯化铯晶体中,每个Cs+周围都紧邻8个Cl—,每个Cl—周围也紧邻8个Cs+
D、在干冰的晶体中,每个CO2分子周围都紧邻4个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用2×10-3 mol的KXO4 恰好将30 mL 0.1 mol·L-1的Na2SO3溶液氧化为Na2SO4,则元素X在还原产物中的化合价是
A.+2 B.+3 C.+4 D.+6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某密闭容器中,可逆反应:A(g) + B(g)![]() xC(g)符合图中(Ⅰ)所示关系:
xC(g)符合图中(Ⅰ)所示关系:![]() (C)表示C气体在混合气体中的体积分数。由此判断,对图像 (Ⅱ) 说法不正确的是:
(C)表示C气体在混合气体中的体积分数。由此判断,对图像 (Ⅱ) 说法不正确的是:

A.p3>p4,Y轴表示A的转化率
B.p3>p4,Y轴表示B的质量分数
C.p3>p4,Y轴表示B的转化率
D.p3>p4,Y轴表示混合气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时向10mL0.1mol·L-1醋酸溶液中不断滴入0.1mol·L-1NaOH溶液,溶液pH变化如图所示。此过程里溶液中离子浓度的关系错误的是
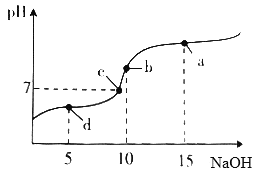
A. a点:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B. b点: c(H+)= c(CH3COOH)+c(OH-)
C. c点:c(Na+)= c(CH3COO-)>c(H+)=c(OH-)
D. d点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸工业中SO2转化为SO3是重要的反应之一,在一定压强和催化剂作用下在2L密闭容器中充入0.8molSO2和2molO2发生反应:2SO2(g)+O2(g)![]() 2SO3(g),SO2的转化率随温度的变化如下表所示:
2SO3(g),SO2的转化率随温度的变化如下表所示:
温度℃ | 450 | 475 | 500 | 525 | 550 | 575 | 600 | 650 |
SO2的转化率% | 97.5 | 95.8 | 95.8 | 93.5 | 90.50 | 85.6 | 80.0 | 73.7 |
(1)能判断该反应是否达到平衡状态的是
A.容器的压强不变
B.混合气体的密度不变
C.混合气体中SO3的浓度不变
D.C(SO2)=C(SO3)
E.v正(SO2)=v正(SO3)
F.v正(SO3)=2v逆(O2)
(2)某温度下经2min反应达到平衡后C(SO2)=0.08mol·L-1,
①此时的温度为 ℃
②若将平衡反应混合物的压强增大1倍(假如体积可变),此时Qc为 (可用分数表示),平衡将 向移动。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com