实验室用下图所示的实验装置制取纯净干燥的无水CuCl2。
| F
(1)检查装置的气密性1分。(2)MnO2+4HCl=MnCl2+Cl2↑+2H2O 2分 ,2.24 2分 (3)饱和食盐水1分,出去氯气中混有的氯化氢气体1分;浓硫酸1分,干燥氯气1分。 (4)Cu+Cl2=CuCl22分,防止F中的水蒸汽进入D中影响实验1分
练习册系列答案
相关习题
科目:高中化学
来源:2012-2013学年新疆布尔津县高中高一分班考试化学试卷(带解析)
题型:实验题
(13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O = 4NaOH+O2↑。以下是某兴趣小组进行的探究活动。
(1)利用如下图所示实验装置制取氧气,请回答有关问题。
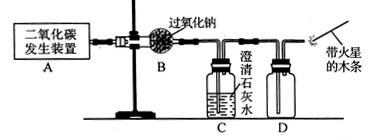
①实验室制取CO2的化学方程式为 。
②表明CO2未被Na2O2完全吸收的实验现象为 。
③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的 性质。
④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进
(2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。
①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是 。
②同学们通过讨论和实验证明了X是Na2CO3。以下是他们设计的有关Na2CO3性质的探究实验,将下表填写完整。
实验操作
| 现 象
| 有关的化学方程式
| 实验一:取少量固体样品,
|
澄清石灰水变浑浊
| Na2CO3+2HCl=2NaCl+H2O+CO2↑
CO2+Ca(OH)2=CaCO3↓+H2O
| 实验二:取少量固体样品,
加水配成溶液,滴加适量的 溶液
|
有白色沉淀产生
|
|
(3)7.8g过氧化钠与足量的水反应,生成氧气的质量是多少?若反应后得到了40g氢氧化钠溶液,请计算氢氧化钠溶液中溶质的质量分数。
查看答案和解析>>
科目:高中化学
来源:2015届新疆布尔津县高中高一分班考试化学试卷(解析版)
题型:实验题
(13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也能跟H2O反应生成O2,化学方程式为:2Na2O2+2H2O
= 4NaOH+O2↑。以下是某兴趣小组进行的探究活动。
(1)利用如下图所示实验装置制取氧气,请回答有关问题。
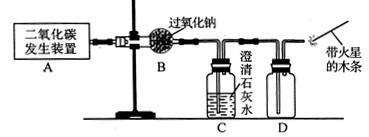
①实验室制取CO2的化学方程式为
。
②表明CO2未被Na2O2完全吸收的实验现象为 。
③O2可采用D装置收集,并用带火星的木条检验,这是利用了O2的 性质。
④若A装置产生的CO2中混有水蒸气,要检验干燥的CO2能否与Na2O2反应生成O2,以上实验装置应如何改进
(2)为探究X是哪种物质及其有关性质,同学们进行了如下分析和实验。
①有同学猜想X可能是酸、碱或盐中的一种。通过对物质组成的分析,大家一致认为X肯定不是酸和碱,理由是
。
②同学们通过讨论和实验证明了X是Na2CO3。以下是他们设计的有关Na2CO3性质的探究实验,将下表填写完整。
|
实验操作
|
现 象
|
有关的化学方程式
|
|
实验一:取少量固体样品,
|
澄清石灰水变浑浊
|
Na2CO3+2HCl=2NaCl+H2O+CO2↑
CO2+Ca(OH)2=CaCO3↓+H2O
|
|
实验二:取少量固体样品,
加水配成溶液,滴加适量的
溶液
|
有白色沉淀产生
|
|
(3)7.8g过氧化钠与足量的水反应,生成氧气的质量是多少?若反应后得到了40g氢氧化钠溶液,请计算氢氧化钠溶液中溶质的质量分数。
查看答案和解析>>
科目:高中化学
来源:
题型:
现代工业将煤炭气化后,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以制成许多清洁能源、扩大水煤气的广泛用途。 (1)已知:①2C(s)+O2(g)=2CO(g) △H1=-221.0kJ.mol-1; ②2H2(g)+O2(g)=2H2O(g)△H2=-483.6kJ.mol-1 则反应C(s)+ H2O(g)= CO(g) + H2(g);△H=____ 。 (2)工业上有一种用CO2 来生产甲醇燃料的方法: CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1 CH3OH(g)+H2O(g) △H=-49.0 kJ·mol-1  现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。 现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。
①下列时间段平均反应速率最大的是______(填序号), A.0~1min B.1~3min C.3~8min D.8~11min 其速率是:υ(H2)=_________ 。 ② 平衡时氢气的转化率 ;该条件下 反应的平衡常数K= 。 ③仅改变某一实验条件再进行两次实验,测得H2的物质的量随时间变化如图中虚线所示,曲线I对应的实验条件改变是___________,曲线II对应的实验条件改变是_____________。 (3)某研究所组装的CH3OH—O2燃料电池的 工作原理如图所示。 
①该电池工作时,b口通入的物质为 , ②该电池正极的电极反应式为: 。  ③以此电池做电源,在实验室中模拟铝制品表面 ③以此电池做电源,在实验室中模拟铝制品表面
“钝化”处理(装置右图所示)的过程中,发现溶液 逐渐变浑浊并有气泡产生,其原因可能是 (用相关的离子方程式表示): 。
查看答案和解析>>
| |
