
【题目】5-羟色胺,最早是从血清中发现的,又名血清素。广泛存在于哺乳动物组织中,是一种抑制性神经递质。下列有关说法正确的是
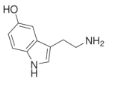
已知:五元氮杂环上的原子在同一平面上。
A.一定共平面的 C 原子有 9 个
B.苯环上的一氯代物有 2 种
C.分子中含有四种官能团,可发生加成、消去、中和等反应
D.5-羟色胺的分子式为 C10H10N2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】配制物质的量浓度为0.1 mol·L-1的Na2CO3溶液100 mL时,下列操作正确的是( )
A. 用托盘天平称取1.06 g无水碳酸钠,在烧杯中加适量水溶解,待冷却到室温后,将溶液转移到容量瓶中
B. 在使用容量瓶前必须检查容量瓶是否完好以及瓶塞处是否漏水
C. 定容时,若加水超过刻度线,可用胶头滴管小心吸出多余部分
D. 定容时,若仰视,则所配溶液的浓度将偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论不正确的是
A.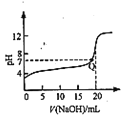 是常温下用0.1000 mol/LNaOH溶液滴定20.000mL 0.l000 mol/L CH3COOH的滴定曲线,说明Q点表示酸碱中和滴定终点
是常温下用0.1000 mol/LNaOH溶液滴定20.000mL 0.l000 mol/L CH3COOH的滴定曲线,说明Q点表示酸碱中和滴定终点
B.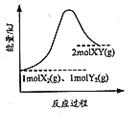 是1mol X2(g)、Imol Y2(g)反应生成2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
是1mol X2(g)、Imol Y2(g)反应生成2mol XY(g)的能量变化曲线,说明反应物所含化学键的键能总和大于生成物所含化学键的键能总和
C.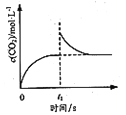 是恒温密闭容器中发生CaCO3(s) = CaO(s)+CO2(g)反应时C(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
是恒温密闭容器中发生CaCO3(s) = CaO(s)+CO2(g)反应时C(CO2)随反应时间变化的曲线,说明t1时刻改变的条件可能是缩小容器的体积
D.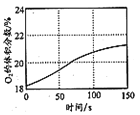 是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照氯水有O2生成
是光照盛有少量氯水的恒容密闭容器时容器内O2的体积分数变化曲线,说明光照氯水有O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述中正确的是
A. 1.00molNaCl中含有NaCl分子数为NA
B. 18gD2O和18gH2O中含有的质子数均为10NA
C. 1molFe高温条件下与水蒸反应,电子转移数为3NA
D. 12g石墨烯(单层石墨)中含有六元环的个数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着科学技术的发展和环保要求不断提高,CO2的捕集利用技术成为研究的重点。
Ⅰ.工业上使用的捕碳剂有NH3和(NH4)2CO3,它们与CO2可发生如下可逆反应:
NH3(l)+H2O(l)+CO2(g)![]() NH4HCO3(aq) ΔH1
NH4HCO3(aq) ΔH1
2NH3(l)+H2O(l)+CO2(g)![]() (NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq) ΔH2
(NH4)2CO3(aq)+H2O(l)+CO2(g)![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3=_________________(用含ΔH1、ΔH2的代数式表示)。
Ⅱ.目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的化学反应方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
CH4(g)+2H2O(g),已知:H2的体积分数随温度的升高而增加。
(1)该反应的ΔS________0(填“>”“<”或“=”),该反应的ΔH________0(填“>”或“<”)。
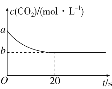
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生上述反应,T ℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示。下列能说明反应达到平衡状态的是________(填字母代号)。
A.体系压强保持不变
B.混合气体密度保持不变
C.甲烷和水蒸气的物质的量之比保持不变
D.H2的质量分数保持不变
(3)T℃下,反应前20 s的平均反应速率v(H2)=______________(用含a、b的代数式表示)。
(4)T℃下,该反应的平衡常数K=_________________________(用含a、b的代数式表示)。
(5)若降低温度,反应重新达到平衡,则v(正)________;CO2转化率________(填“增大”“减小”或“不变”)。
Ⅲ.工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图所示:
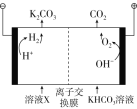
(1)在阳极区发生的反应包括___________________________________和H++HCO3-=CO2↑+H2O。
(2)简述CO32-在阴极区再生的原理:____________________________。
(3)NH3·BH3+3H2O2=NH4BO2+4H2O。下列说法正确的是___________。
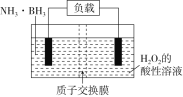
A.电流从左侧电极经过负载后流向右侧电极
B.BO2-通过质子交换膜向正极移动
C.负极附近溶液pH增大
D.正极的反应式为3H2O2+6H++6e-=6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,反应HCO3-+H2O![]() H2CO3+OH-的平衡常数为10-8 。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
H2CO3+OH-的平衡常数为10-8 。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
A.0.2mol/L 氨水:c(NH3H2O)>c(NH4+)>c(OH-)>c(H+)
B.0.6 mol/L氨水和0.2 mol/L![]() 溶液等体积混合:c(NH3H2O)+c(CO32-)+c(OH-)=0.3mol/L+2c(H2CO3)+c(H+)
溶液等体积混合:c(NH3H2O)+c(CO32-)+c(OH-)=0.3mol/L+2c(H2CO3)+c(H+)
C.0.2 mol/L氨水和0.2 mol/L![]() 液等体积混合:c(NH4+)+c(NH3H2O)=c(H2CO3)+c(HCO3-)+c(CO32-)
液等体积混合:c(NH4+)+c(NH3H2O)=c(H2CO3)+c(HCO3-)+c(CO32-)
D.0.2mol/L NH4HCO3溶液(pH>7):c(NH4+)>c(HCO3-)>c(H2CO3)>c(NH3H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是几种苯的同系物,回答下列问题:
①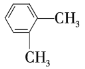 ②
②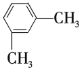 ③
③![]() ④
④![]() ⑤
⑤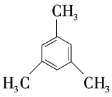 ⑥
⑥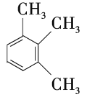 ⑦
⑦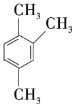
(1)①②③之间的关系是______。
(2)按习惯命名法命名,②的名称为______;按系统命名法命名,③⑥的名称分别为______、______。
(3)以上7种苯的同系物中苯环上的一氯代物只有一种的是______(填序号),④苯环上的一氯代物有______种。
(4)④的同分异构体有多种,除⑤⑥⑦外,写出苯环上一氯代物有2种,且与④互为同分异构体的有机物的结构简式:______,它的系统名称为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素及其衍生物在医药、农药、染科等领域有广泛用途。某香豆素衍生物Ⅰ具有抗病毒、抗癌的动多种生物活性,其合成路线如图所示:
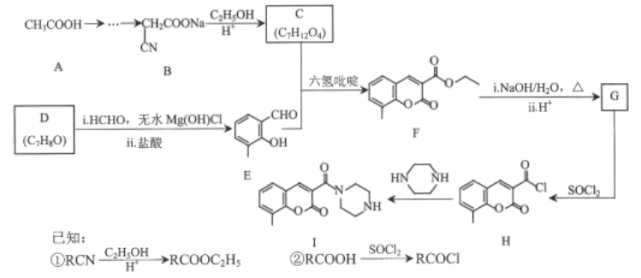 回答下列问题:
回答下列问题:
(1)D的名称是______。F中的含氧官能团的名称是______。
(2)H→I的反应类型为______。
(3)C分子具有对称结构,该化合物的结构简式为______。
(4)F→G中i的化学方程式为______。
(5)E的同分异构体中,满足下列条件的有______种;
①含有苯环
②能发生水解反应
其中核磁共振氢谱有4组峰且峰面积之比为3:2:2:1的结构简式为______(写出一种即可)。
(6)根据上述路线,设计以苯酚、乙醇、丙二酸、甲醛为原料制备![]() 的合成路线______(其他无机试剂自选)。
的合成路线______(其他无机试剂自选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量CO2) 直接制备二甲醚,其中的主要过程包括以下四个反应:
①CO(g)+2H2(g)![]() CH3OH(g) ΔH1=-90.1kJ·mol-1
CH3OH(g) ΔH1=-90.1kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ΔH2=-49.0kJ·mol-1
CH3OH(g)+H2O(g) ΔH2=-49.0kJ·mol-1
③CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3=+41.1kJ·mol-1
CO(g)+H2O(g) ΔH3=+41.1kJ·mol-1
④2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH4=-24.5kJ·mol-1。试回答下列问题:
CH3OCH3(g)+H2O(g) ΔH4=-24.5kJ·mol-1。试回答下列问题:
(1)由H2和CO直接制备二甲醚的热化学方程式:2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) ΔH =_______kJ·mol-1;该反应可以自发进行的条件为________________。
CH3OCH3(g)+H2O(g) ΔH =_______kJ·mol-1;该反应可以自发进行的条件为________________。
(2)将1.0mol CO2 和 3.0mol H2 充入2L恒容密闭容器中,使其仅按反应②进行,在不同催化剂作用下,相同时间内 CO2 的转化率随温度变化如图所示。下列说法正确的是______________
A.T3对应的平衡常数小于T4对应的平衡常数
B.根据图中曲线分析,催化剂I的催化效果最好
C.b点v(正)可能等于v(逆)
D.a点的转化率比c点高可能的原因是该反应为放热反应,升温平衡逆向移动,转化率降低
(3)若CO2和H2仅发生反应②和③,研究表明:在其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性,使用该催化剂,按 n(CO2):n(H2)=1:3(总量为a mol)投料于恒容密闭容器中进行反应,CO2的平衡转化率和甲醇的选择率(甲醇的选择率:转化的 CO2中生成甲醇的物质的量分数)随温度的变化趋势如图所示:(忽略温度对催化剂的影响)
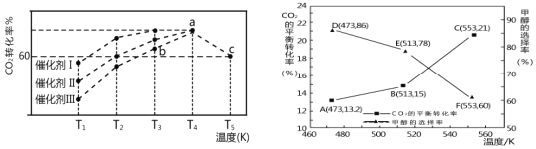
①在553K达到平衡时,反应体系内甲醇的物质的量为_________mol。
②随着温度的升高,CO2的平衡转化率增加但甲醇的选择率降低,请分析其原因:____________________________ 。
(4)O2催化辅助的 Al-CO2电池工作原理如图所示。该电池电容量大,能有效利用CO2,电池反应产物Al2(C2O4)3是重要的化工原料。 则电池的正极反应式:6O2+6e-=6O2-和____________________ 。
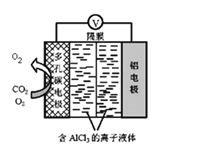
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com