
【题目】I.“洁净煤技术”研究在世界上相当普遍,科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,连续产出了高热值的煤炭气,其主要成分是CO和H2。CO和H2可作为能源和化工原料,应用十分广泛.生产煤炭气的反应之一是:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.4kJ/mol
CO(g)+H2(g) △H=+131.4kJ/mol
(1)在容积为3L的密闭容器中发生上述反应,5min后容器内气体的密度增大了0.12g/L,用H2O表示0~5min的平均反应速率为 。
(2)关于上述反应在化学平衡状态时的描述正确的是 .
A.CO的含量保持不变 B.v正(H2O)=v正(H2)
C.容器中混合气体的平均相对分子质量保持不变
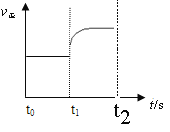
(3)若上述反应在t0时刻达到平衡(如图),在t1时刻改变某一条件,请在图中继续画出t1时刻之后正反应速率随时间的变化:

①缩小容器体积,t2时到达平衡(用实线表示);
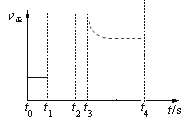
②t3时平衡常数K值变大,t4到达平衡(用虚线表示)。
(4)在一定条件下用CO和H2可以制得甲醇(化学式为CH3OH),CH3OH和CO的燃烧热分别为725.8kJ/mol,283.0kJ/mol,1molH2O(l)变为H2O(g)吸收44.0 kJ的热量,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式 。
II.实施以减少能源浪费和降低废气排放为基本内容的节能减排政策,是应对全球气候问题、建设资源节约型、环境友好型社会的必然选择。化工行业的发展必须符合国家节能减排的总体要求。试运用所学知识,解决下列问题:
(1)已知某反应的平衡常数表达式为:![]() ,它所对应的化学方程式为 。
,它所对应的化学方程式为 。
(2)已知在400℃时,N2(g)+3H2(g)![]() 2NH3(g)△H<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正 V(N2)逆(填:>、<、=、不能确定)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是 (填序号)
2NH3(g)△H<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(N2)正 V(N2)逆(填:>、<、=、不能确定)。欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积百分数增加,可采取的正确措施是 (填序号)
A、缩小体积增大压强 B、升高温度 C、加催化剂 D、使氨气液化移走
【答案】I.(1)0.002mol/(L·min);(2)ABC;(3)各1分
(4)CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8kJ/mol
Ⅱ(1)C(s)+H2O(g)![]() H2(g)+CO(g)(可不标状态)(2)=;A
H2(g)+CO(g)(可不标状态)(2)=;A
【解析】
试题分析:I.(1)因为是等体积,因此密度增大了0.12g·L-1,气体质量增大了3×0.12g=0.36g,根据质量差,求出消耗的H2O的物质的量0.36/12mol=0.03mol,v(H2O)=0.03/(3×5)mol/(L·min)=0.002 mol/(L·min);
(2)A、根据化学平衡状态的定义,CO的含量保持不变,说明反应达到平衡,A正确;B、v正(H2O)=v正(H2),说明正逆反应速率相等,反应达到平衡状态,B正确;C、根据摩尔质量的定义,气体的质量增大,气体的物质的量增大,因此摩尔质量不变,说明反应达到平衡,C正确,答案选ABC;
(3)①缩小容器的体积,增大压强,根据勒夏特列原理,平衡向逆反应方向移动,图像是: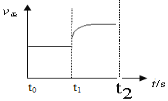 ;
;
②平衡常数增大,只改变温度,说明化学反应向正反应方向移动,此反应是吸热反应,因此升高温度,图像是: ;
;
(4)①CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=-725.8kJ·mol-1,②CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ·mol-1,③H2O(l)=H2O(g) △H=+44.0kJ·mol-1,CH3OH+O2=CO+2H2O(g),根据盖斯定律可知①-②+2×③得出:CH3OH(l)+O2(g)=CO(g)+2H2O(g) △H=(-725.8+283+2×44)kJ·mol-1=-354.8kJ·mol-1;
Ⅱ、(1)反应的平衡表达式为:![]() ,依据平衡常数概念和原子守恒,它所对应的化学方程式为:C(s)+H2O(g)
,依据平衡常数概念和原子守恒,它所对应的化学方程式为:C(s)+H2O(g)![]() H2(g) + CO(g);
H2(g) + CO(g);
(2)在400℃时,反应N2(g)+3H2(g)![]() 2NH3(g)△H<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,反应的Qc=
2NH3(g)△H<0的K=0.5,则400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,反应的Qc=![]() =0.5=K,说明反应达到平衡状态,v(N2)正=v(N2)逆;欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,可采取的正确措施是让化学平衡正向进行;A、反应是气体体积减小的反应,缩小体积增大压强,反应速率增大,平衡正向进行,NH3的体积分数增加,A正确;B、反应是放热反应,升高温度速率增大,平衡逆向进行,B错误;C、加催化剂改变化学反应速率,不改变化学平衡,C错误; D.使氨气液化移走,平衡正向进行,反应速率减小,D错误。答案选A。
=0.5=K,说明反应达到平衡状态,v(N2)正=v(N2)逆;欲使得该反应的化学反应速率加快,同时使平衡时NH3的体积分数增加,可采取的正确措施是让化学平衡正向进行;A、反应是气体体积减小的反应,缩小体积增大压强,反应速率增大,平衡正向进行,NH3的体积分数增加,A正确;B、反应是放热反应,升高温度速率增大,平衡逆向进行,B错误;C、加催化剂改变化学反应速率,不改变化学平衡,C错误; D.使氨气液化移走,平衡正向进行,反应速率减小,D错误。答案选A。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)。
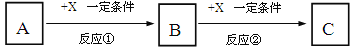
(1)若X是空气中存在的强氧化性无色气体单质,则A可能是___________(填序号)
a.C b.N2 c.S d.Al
(2)若X是日常生活中最常用的金属单质,A是气体单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀HNO3的白色沉淀,X在气体A中燃烧产生棕黄色的烟。
B的化学式为____________; 反应②的化学方程式为:___________________,
C溶液中加入NaOH溶液后产生的现象是_________________________, 方程式为____________________________________、_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用铁片和稀硫酸反应制氢气时,下列措施不能使氢气生成速率加快的是( )
A.水浴加热
B.将稀硫酸改为98%的浓硫酸
C.滴加少许CuSO4溶液
D.改用铁粉并振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个2L的密闭容器中投入反应物,发生反应2SO3(g)![]() 2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:
2SO2(g)+O2(g)△H>0,其中SO3的变化如图所示:
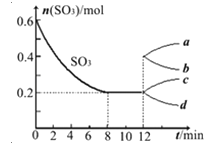
(1)根据8min时到达平衡,算出该反应的平衡常数值为 。
(2)用O2表示0到8min内该反应的平均速率v= 。
(3)能说明该反应已达到平衡状态的是 。
A、v(SO3)=2v(O2)
B、容器内压强保持不变
C、v(SO2)逆=2v(O2)正
D、容器内密度保持不变
(4)在第12min时,容器压缩到1L,则SO3的变化曲线为 。
A、a B、b C、c D、d
(5)若保持容积不变在第12min时,加入SO3(g),则平衡向 反应方向移动(填“正”或“逆”)。SO3的体积分数 (填“增大”或“减小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应,硼与氯气反应生成三氯化硼(BC13),生成的三氯化硼遇水水解产生白雾(已知:BC13的熔点为-107. 3℃,沸点为12.5 ℃),且三氯化硼用于制取乙硼烷(B2H6)。某兴趣小组设计如图所示装置制备三氯化硼。
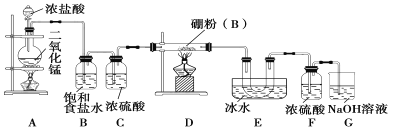
回答下列问题:
(1)装置D中发生反应的化学方程式为_____________________。
(2)装置B、E的作用分别是________________、________________。
(3)可以用盛装____________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
(4)为了顺利完成实验,点燃酒精灯的正确操作是______(填字母),其理由是__________。
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方法中,不能用于实验室制取氨的是
A. 在烧瓶中将熟石灰和氯化铵混合,加水调成泥状后加热
B. 加热试管中的氯化铵固体
C. 将烧瓶中的浓氨水加热
D. 将分液漏斗中的浓氨水滴入装有生石灰的烧瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下图所示的转化关系(部分产物及反应条件已略去),下列判断正确的是( )
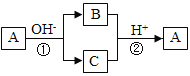
A. X元素不一定为非金属元素
B. 单质A可能是Cl2不能是S
C. 反应①和②一定为氧化还原反应
D. 反应①和②互为可逆反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊是五种短周期原子序数依次递增的主族元素,乙、丁、戊在周期表的相对位置如右图。甲能与丙形成四核10电子的分子,则下列说法正确的是( )
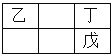
A. 丙的非金属性强,丙单质的氧化性也强
B. 甲与乙、甲与丁都能形成原子个数比1: 1和2:1的分子
C. 丁的氢化物沸点高于戊的氢化物沸点说明丁的非金属性比戊强
D. 简单阴离子还原性:丁>戊,简单阴离子半径:丁>丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质或应用正确的是
A. 单质硅用于制造芯片和光导纤维
B. 浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性
C. SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色
D. 30%的H2O2溶液中加入MnO2可制得O2,MnO2做氧化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com