

分析 (1)制备气体的仪器连接遵从发生装置→除杂装置→干燥装置→收集→尾气吸收的顺序,考虑制备氯气中含有HCl和水蒸气等杂质气体,所以先用排饱和食盐水法除去HCl,再用浓硫酸吸收水蒸气,再用向上排空气法收集,用碱吸收尾气,据此进行解答;
(2)根据图中的发生装置可知,该实验中采用了难挥发的硫酸制备挥发性的盐酸,再与二氧化锰制备氯气的方法;
(3)①加入的试剂是NH3•H2O可以使Fe3+沉淀除去,除去SO42-需要加入Ba2+试剂,使之转化为BaSO4沉淀除去,结合不引入过多杂质判断选用试剂;为了把NH4+除去,可以加入强碱KOH;
②步骤c中除去的是杂质Br-,所以加入新制氯水;
(4)①甲同学已经假设是FeSO4与HNO3作用,所以根据提供的资料可以猜测导致实验现象的可能是SCN-和硝酸作用的结果;
②如果按照甲同学的假设分析,FeSO4与HNO3作用只会导致Fe2+被氧化为Fe3+最终和KSCN作用使溶液变红,且加入的浓HNO3过量,不会出现溶液显红色后又变成蓝色;
③根据乙同学的假设,造成实验现象的是浓HNO3和KSCN溶液作用的结果.根据物质中的元素组成分析,浓硝酸生成红棕色气体NO2,SCN-中产生的能使Ba(OH)2溶液产生浑浊现象的气体不可能是SO2,因为SO2容易被强氧化剂氧化,所以只可能是CO2,而S被氧化为SOSO42-在反应后的溶液中,所以加入BaCl2溶液能产生白色沉淀;剩余的空气主要成分的气体是N2;
④用SCN-间接检验Fe2+时,需要加入强氧化剂把Fe2+氧化才会出现无色变红色现象,但是根据上述中的实验经历,如果强氧化剂过量容易把用SCN-氧化,使溶液红色消失变成蓝色;根据资料提供显示氧化性Cl2>(SCN)2,所以氯气过量同样能氧化SCN-,造成红色消失变成蓝色的现象,则加入氧化剂的量必须要少量.
解答 解:(1)制备气体的仪器连接遵从发生装置→除杂装置→干燥装置→收集→尾气吸收的顺序,考虑制备氯气中含有HCl和水蒸气等杂质气体,所以先用排饱和食盐水法除去HCl,再用浓硫酸吸收水蒸气,再用向上排空气法收集,用碱吸收尾气,满足该顺序,连接应为H→B、A→C、D→E,所以根据顺序可以得知广口瓶Ⅱ中的试剂为饱和食盐水,
故答案为:H→B、A→C、D→E;饱和食盐水;
(2)根据图中的发生装置可知,该实验中采用了难挥发的硫酸制备挥发性的盐酸,再与二氧化锰制备氯气的方法,所以方程式为:2NaCl+MnO2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$MnSO4+Na2SO4+2H2O+Cl2↑,
故答案为:2NaCl+MnO2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$MnSO4+Na2SO4+2H2O+Cl2↑;
(3)①氯化钾中含有Fe3+、SO42-、Br-等杂质离子,其中加入的试剂是NH3•H2O可以使Fe3+沉淀除去,除去SO42-需要加入Ba2+试剂,使之转化为BaSO4沉淀除去,为了不引入过多杂质,应选用阴离子相同的BaCl2;为了把NH4+除去,可以加入强碱KOH,所以步骤a中依次加入的试剂是NH3•H2O、BaCl2、KOH,
故答案为:BaCl2、KOH;
②步骤c中除去的是杂质Br-,所以加入新制氯水,把Br-转化为单质Br2除去,
故答案为:足量的新制氯水;
(4)①甲同学已经假设是FeSO4与HNO3作用,所以根据提供的资料可以猜测导致实验现象的可能是SCN-和硝酸作用的结果,所以乙同学假设是SCN-与HNO3作用,
故答案为:SCN-;
②如果按照甲同学的假设分析,FeSO4与HNO3作用只会导致Fe2+被氧化为Fe3+最终和KSCN作用使溶液变红,且加入的浓HNO3过量,不会出现溶液显红色后又变成蓝色,所以甲同学假设不成立,
故答案为:HNO3过量,没有Fe2+剩余;
③根据乙同学的假设,造成实验现象的是浓HNO3和KSCN溶液作用的结果.根据物质中的元素组成分析,浓硝酸生成红棕色气体NO2,SCN-中产生的能使Ba(OH)2溶液产生浑浊现象的气体不可能是SO2,因为SO2容易被强氧化剂氧化,所以只可能是CO2,而S被氧化为SOSO42-在反应后的溶液中,所以加入BaCl2溶液能产生白色沉淀;剩余的空气主要成分的气体是N2,所以产生的气体依次是NO2、CO2、N2,
故答案为:NO2、CO2、N2;
④用SCN-间接检验Fe2+时,需要加入强氧化剂把Fe2+氧化才会出现无色变红色现象,但是根据上述中的实验经历,如果强氧化剂过量容易把用SCN-氧化,使溶液红色消失变成蓝色.根据资料提供显示氧化性Cl2>(SCN)2,所以氯气过量同样能氧化SCN-,造成红色消失变成蓝色的现象,所以加入氧化剂的量必须要少量,
故答案为:少量.
点评 本题考查的是探究性试验与实验室制备氯气、离子的除杂和亚铁离子的检验相结合的实验题,题目浓度较大,明确实验目的、实验原理为解答关键,试题知识点较多、综合性较强,充分考查了学生的分析、理解能力及化学实验能力.


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; .
. .
.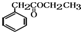 )的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
)的合成路线流程图(无机试剂任选).合成路线流程图示例如下: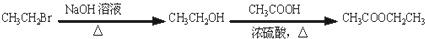
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池工作时两极质量均增加 | |
| B. | Fe上镀Ag时,Ag接电源的正极 | |
| C. | 精炼铜时,阳极有0.2 molCu氧化阴极就有0.1 molCu2+被还原 | |
| D. | 用惰性电极电解饱和NaCl溶液和KNO3溶液,阴极都得到H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 立即撤离火灾现场并拨打119报警 | |
| B. | 若逃生通道被堵,应迅速转移到窗口边或阳台上等待救援 | |
| C. | 若被困在室内,应立即封堵火、烟的进口,并站在室内最高处等待救援 | |
| D. | 若被困在火灾现场,应尽可能贴近地面向火势小、烟雾少的方向撤离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅不与酸溶液反应,可用石英器皿盛放氢氟酸 | |
| B. | 分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 | |
| C. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 | |
| D. | 将过量的CO2通入次氯酸钙溶液可生成次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2 是酸性氧化物,能与NaOH溶液反应 | |
| B. | Na2O、Na2O2组成元素相同,与 CO2反应产物也相同 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 通过化学变化可以实现16O与18O间的相互转化 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
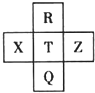 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R单质在暗处与H2剧烈化合并发生爆炸.则下列判断正确的是( )| A. | 非金属性:Z<T<X | |
| B. | X最高价氧化物的水化物的表达式为H2XO4 | |
| C. | 气态氢化物稳定性:R<T<Q | |
| D. | R与Q的电子数相差26 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com