
【题目】利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO、SiO2等)可以制取多种化工试剂。下图是草酸钴晶体和氯化钴晶体的制备流程,回答下列问题:
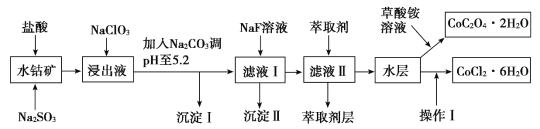
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等。
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中Co2O3发生反应的离子方程式为______________。
(2)1molNaClO3在浸出液中发生反应时,转移的电子数为_________。
(3)加入Na2CO3调pH至5.2只得到两种沉淀,则沉淀I的成分为______________(填化学式,下同);萃取剂层含锰元素,则沉淀Ⅱ的主要成分为______________。
(4)操作Ⅰ包括:将水层加入浓盐酸调整pH为2~3、________、________、过滤、洗涤、减压烘干等过程。
(5)将5.49g草酸钴晶体(CoC2O4·2H2O)置于空气中加热,受热过程中,不同温度范围内得到一种不同的固体物质,其质量如表。
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
经测定,整个受热过程产生的气体只有水蒸气和CO2,则290~320℃范围内,剩余固体物质的化学式为______________。
【答案】Co2O3+SO32-+4H+===2Co2++SO42-+2H2O 6NA或3.612×1024 Fe(OH)3、Al(OH)3 CaF2、MgF2 蒸发浓缩 冷却结晶 Co3O4(或CoO·Co2O3)
【解析】
含钴废料中加入盐酸,可得到CoCl3、FeCl3、AlCl3、MnCl2、MgCl2、CaCl2,根据信息①中浸出液中含有的阳离子只要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等,则进入的Na2SO3将Co3+、Fe3+还原为Co2+、Fe2+。工艺流程最终为草酸钴,NaClO3将Fe2+氧化为Fe3+,加入Na2CO3调pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,过滤后得到的滤液主要含有CoCl2、MnCl2、CaCl2,用NaF溶液出去Ca、Mg,过滤后向滤液中加入萃取剂,将Mn2+萃取,萃取后的溶液中主要含有CoCl2,加入草酸铵溶液得到草酸钴。
(1)根据上述分析可知浸出过程中Co2O3发生的离子反应为:Co2O3+SO32-+4H+===2Co2++SO42-+2H2O;
(2)NaClO3具有氧化性,能将Fe2+氧化成Fe3+,自身还原成Cl-,离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O,根据方程式可知1molNaClO3在浸出液中发生反应时,转移的电子数为6NA;
(3)根据上述分析可知,加入Na2CO3调节pH的目的是使Fe3+和Al3+沉淀完全;沉淀Ⅱ的主要成分为CaF2和MgF2;
(4)操作Ⅰ包括:将水层加入浓盐酸调整pH至2-3,蒸发浓缩、冷却结晶、过滤、洗涤、减压烘干等过程;
(5)5.49g草酸钴晶体的物质的量是0.03mol,分解生成水的质量是1.08g,所以150-210℃时失水,剩余固体是CoC2O4;290-320℃时剩余固体中Co的质量是1.77g,氧原子是质量是2.41g-1.77g=0.64g,物质的量为0.64/16=0.04mol,则剩余固体中Co原子与O原子的物质的量比为3:4,所以化学式为Co3O4。


科目:高中化学 来源: 题型:
【题目】反应A+B![]() C(ΔH < 0)分两步进行:①A+B
C(ΔH < 0)分两步进行:①A+B![]() X(ΔH>0); ②X
X(ΔH>0); ②X![]() C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是( )。
A.
B.
C.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如图所示。
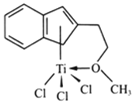
①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
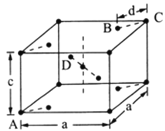
①A、B、C、D4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。
③若晶胞底边长为a cm,高为c cm,则TiO2晶体的密度为______g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项中I、II两个反应属于同一反应类型的是( )
选项 | 反应I | 反应II |
A |
| CH2=CH2→CH3CH2Cl |
B | CH3CH2Cl→CH3CH2OH | CH3CH2OH→CH3COOCH2CH3 |
C | CH3CH2OH→CH2=CH2 | CH3CH2OH→CH3CHO |
D | 油脂→甘油 |
|
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机合成在工业上有着广泛的应用。工业上由化合物A进行的一种合成路线如下:
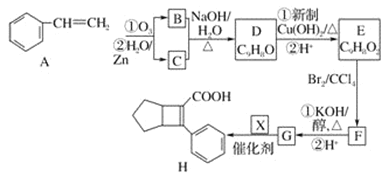
已知:①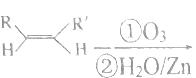 RCHO+RCHO
RCHO+RCHO
②RCHO+RCH2CHO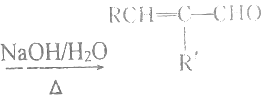 +H2O
+H2O
③
请回答下列问题:
(1)化合物A所含官能团名称为_________,芳香化合物B的名称为_________,C的同系物中相对分子质量最小的结构简式为__________。
(2)由E生成F的反应类型为_________。
(3)X的结构简式为_________。
(4)写出D生成E的第①步反应的化学方程式_______________。
(5)G与乙醇发生酯化反应生成化合物Y,Y有多种同分异构体,其中符合下列条件的同分异构体有____种,写出其中任意一种的结构简式________。
①分子中含有苯环,且能与饱和碳酸氢钠溶液反应放出CO2;
②其核磁共振氢谱显示有4种不同化学键环境的氢,且峰面积之比为6:2:1:1。
(6)写出用![]() 为原料制备化合物
为原料制备化合物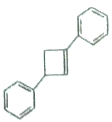 的合成路线,其他无机试剂任选。________
的合成路线,其他无机试剂任选。________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,5-二羟基苯甲酸甲酯俗称龙胆酸甲酯,可由龙胆酸与甲醇酯化得到,是合成制药中的常见中间体。其结构如图所示。
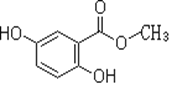
回答以下问题:
(1)龙胆酸甲酯的分子式为__________
(2)下列有关龙胆酸甲酯的描述,正确的是_____(填字母)。
a.能发生消去反应 b.能与氢气发生加成反应 c.能与浓溴水反应
(3)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式_________ 。
(4)写出满足下列条件的龙胆酸的两种同分异构体的结构简式_______、_______。
①能发生银镜反应; ②能使FeCl3溶液显色;
③酯类 ④苯环上的一氯代物只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组用下列装置完成了探究浓硫酸和 SO2性质的实验(部分夹持装置已省略),下列“ 现象预测” 与“ 解释或结论” 均正确的是
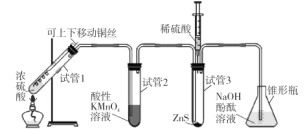
选项 | 仪器 | 现象预测 | 解释或结论 |
A | 试管1 | 有气泡、酸雾,溶液中有白色固体出现 | 酸雾是SO2所形成,白色固体是硫酸铜晶体 |
B | 试管2 | 紫红色溶液由深变浅,直至褪色 | SO2具有还原性 |
C | 试管3 | 注入稀硫酸后,没有现象 | 由于Ksp(ZnS)太小,SO2与ZnS在注入稀硫酸后仍不反应 |
D | 锥形瓶 | 溶液红色变浅 | NaOH溶液完全转化为NaHSO3溶液,NaHSO3溶液碱性小于NaOH |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】银精矿主要含有 Ag2S(杂质是铜、锌、锡和铅的硫化物),工业上利用银精矿制取贵金属银,流程图如下图所示。已知“ 氯化焙烧” 能把硫化物转化为氯化物,请回答下列问题:

(1)“ 氯化焙烧” 的温度控制在 650~670℃,如果温度过高则对焙烧不利,产率会降低,原因是 ______。
(2)水洗后的滤液中溶质有盐酸盐和大量钠盐,取少量滤液加入盐酸酸化,再滴入氯化钡溶液有白色沉淀生成,此钠盐为_____(填化学式)。
(3)氨浸时发生的化学反应方程式为________。
(4)“ 沉银” 是用 N2H4还原银的化合物。
①N2H4的电子式是_______。
②理论上,1molN2H4完全反应所得到的固体质量是______g。
③向所得母液中加入烧碱,得到的两种物质可分别返回________ 、______工序中循环使用。
(5)助熔剂 Na2CO3和 Na2B4O7有两个作用:一是降低了银的熔点,减少能耗;二是____。利用________的方法可以进一步直接精炼银锭。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水加工处理流程如图,下列有关说法不正确的是( )

A.若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池
B.投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3﹣等
C.自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染
D.用ClO2消毒自来水,消毒效率是等质量氯气的2.63倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com