
【题目】对于常温下pH=2的醋酸溶液,下列叙述正确的是( )
A.由水电离产生的c(H+)=10-2mol/L
B.加水稀释时![]() 增大
增大
C.与pH=12的NaOH溶液等体积混合后,溶液呈中性
D.与pH=2的盐酸相比,醋酸中H+浓度更大
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
【题目】(1)电化腐蚀是钢铁发生腐蚀的主要原因,当水膜氢离子浓度较小时,主要发生________腐蚀,其负极反应式为____________________,正极反应式为______________________。
(2)将氯化铁溶液蒸干灼烧得到的固体物质是______;(填化学式,下同)将硫酸铝溶液蒸干得到的固体物质是___________________ 。
(3)除CaSO4水垢的方法,写出反应的化学方程式_________________、_________________;热的纯碱溶液洗涤效果更好的原理是_________________________;明矾净水的离子方程式__________________。
(4)在2 mL 0.1 mol·L-1的NaCl溶液中,加入2 mL 0.1 mol·L-1的AgNO3溶液,可观察到______________,此反应的离子方程式为_________。将此混合液过滤,滤渣加入2 mL 0.1 mol·L-1的KI溶液,搅拌,可观察到____,反应的离子方程式为________。
(5)对于Ag2S(s)![]() 2Ag+(aq)+S2-(aq),其Ksp的表达式为_______。
2Ag+(aq)+S2-(aq),其Ksp的表达式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香族化合物A(![]() )是重要的有机化工原料。由A制备有机化合物F的合成路线(部分反应条件略去)如下图所示:
)是重要的有机化工原料。由A制备有机化合物F的合成路线(部分反应条件略去)如下图所示:

(1)A的分子式是______,B含有的官能团的名称是_________。
(2)D→E的反应类型是_________。
(3)已知G能与金属钠反应,则G的结构简式为________。
(4)写出E→F的化学方程式:_________。
(5)龙胆酸D的同分异构体有多种,符合下列条件的有___种。写出其中一种核磁共振氢谱有六组峰的同分异构体的结构简式:____。
①能发生银镜反应;②与FeCl3溶液发生显色反应;③1mol该物质能与2mol Na2CO3反应。
(6)已知: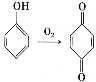 。参照上述合成路线,设计一条以苯酚、乙醇为原料制备龙胆酸乙酯(
。参照上述合成路线,设计一条以苯酚、乙醇为原料制备龙胆酸乙酯(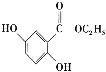 )的合成路线(无机试剂任用)。_________
)的合成路线(无机试剂任用)。_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】传感器可以检测空气中SO2的含量,传感器工作原理如下图所示。下列叙述正确的是( )

A.b为电源的正极
B.负极反应式 Ag - e- + Cl- = AgCl
C.当电路中电子转移为5×10-5 mol时进入传感器的SO2为 1.12 mL
D.阴极的电极反应式是2HSO3-+2H++2e-= S2O42-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄是一种常见水果,可以生食或制作葡萄干,除此之外,葡萄还可用于酿酒。
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是________。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)![]() 2_________+ 2 C2H5OH
2_________+ 2 C2H5OH
(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是__________。
②试管b中盛放的试剂是饱和____________溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是________。
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是_______(填字母)。
A.普通漏斗 B.分液漏斗 C.长颈漏斗
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。下列有关说法正确的是( )

A.反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B.乙装置中铁电极为阴极,电极反应式为Fe-2e-=Fe2+
C.甲中通入氧气的一极为阳极,发生的电极反应为O2+4e-+2H2O=4OH-
D.反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近期发现,H2S是继NO、CO之后的第三个生命体系气体信号分子,它具有参与调节神经信号传递、舒张血管减轻高血压的功能。常温时,H2S在水中的电离常数Ka1=1.3×10-7,Ka2=7.0×10-15。按要求回答下列问题:
(1)H2S在水中的二级电离常数表达式Ka2=______;0.1mol/LNa2S溶液中离子浓度由大到小的顺序为__________.
(2)常温下,向0.1mol/LH2S溶液中通入HCl或加入NaOH固体,测得c(S2-)与溶液pH的关系如图(忽略溶液体积的变化及H2S的挥发)。

①当溶液中c(S2-)=1.4×10-19mol/L时,溶液中c(OH-)=______,水电离产生的c(H+)=______.
②当pH=13时,溶液中的c(H2S)+c(HS-)=_______.
(3)在工业废水处理中常用H2S将Mn2+转化为MnS除去。常温下,向含有0.010mol·L-1 Mn2+废水中通入H2S以调节废水的pH,当c(HS-)=2.0×10-4mol·L-1时,Mn2+开始沉淀,此时废水的pH=___。[已知Ksp(MnS)=1.4×10-15]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是

A. K与N连接时,X为硫酸,一段时间后溶液的pH增大
B. K与N连接时,X为氯化钠,石墨电极反应:2H++2e-=H2↑
C. K与M连接时,X为硫酸,一段时间后溶液的pH增大
D. K与M连接时,X为氯化钠,石墨电极反应:4OH--4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高分子材料的结构如图所示:已知该高分子材料是由三种单体聚合而成的,以下与此高分子材料相关的说法正确的是( )

A.三种单体中有两种有机物互为同系物
B.三种单体都可以使溴水褪色,但只有两种能使酸性高锰酸钾溶液褪色
C.形成该高分子材料的单体![]() 中,所有原子一定处于同一平面
中,所有原子一定处于同一平面
D.该高分子材料是体型高分子,合成它的反应是加聚反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com