
 工业上制纯碱的方法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱(纯碱样品中Na2CO3的质量分数为92%~96%)。涉及到的化学方程式有:
工业上制纯碱的方法是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得碳酸氢钠晶体加热分解后即可得到纯碱(纯碱样品中Na2CO3的质量分数为92%~96%)。涉及到的化学方程式有:
NH3+CO2+H2O → NH4HCO3,NH4HCO3+NaCl(饱和)→ NaHCO3↓+NH4Cl,![]() 。请回答:
。请回答:
(1)工业制得的纯碱中常常含有少量的氯化钠杂质,其主要原因是 。
(2)现有甲、乙、丙三个学生,欲测定某工业纯碱样品中Na2CO3的质量分数,分别设计如下方案,请你帮助他们完成如下实验。
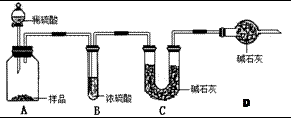
甲:用 (填实验仪器)称取10.0g样品,利用上图所示装置,测出反应后装置C中碱石灰增重3.52g。装置D中碱石灰的作用是 。
乙:准确称取10.00g样品后,用 (填实验仪器)配成1000mL溶液,用
式滴定管量取25.00mL放入锥形瓶中,加入2滴酚酞作指示剂,用0.15mol·L-1的标准盐酸溶液滴定至终点(有关反应为Na2CO3+HCl → NaCl+NaHCO3)。完成三次平行实验后,消耗盐酸体积的平均值为15.00mL。
丙:准确称取10.00g样品后,向其中加入过量的盐酸,充分反应直至样品中无气泡冒出,蒸干混合溶液将所得到固体物质于干燥器中冷却至室温后称量。反复加热、冷却、称量,直至所称量的固体质量几乎不变为止,此时所得固体的质量为10.99g。请分析、计算后填表:
| 分析与计算 分组 | 计算样品中碳酸钠的质量分数 | 实验结果的评价 | 实验失败的主要原因及对结果的影响 |
| 甲 |
| 失 败 | |
| 乙 |
|
| |
| 丙 |
|
|
(1)在饱和氯化钠溶液中通入氨气和二氧化碳后,发生反应NH3+CO2+H2O=NH4HCO3,消耗了部分水,从而会有部分氯化钠晶体析出 (2分)
(2)甲:托盘天平、药匙、滤纸(共2分,少一个扣0.5分) 防止空气中的水蒸气和二氧化碳进入C,减小实验误差 (2分)
乙:烧杯、玻璃棒、胶头滴管、1000mL 的容量瓶(2分) 碱 (1分)
丙:(共8分,每空2分)
| 计算样品中碳酸钠的质量分数 | 实验失败的主要原因及对结果的影响 |
| 84.8% | 反应生成的CO2部分残留在瓶A中,没有被完全吸收,结果偏小 |
| 95.4% | |
| 95.4% |
(1)因NaCl形成饱和溶液,析出NaCl晶体应该与溶剂H2O减少有关,当饱和NaCl溶液中通入NH3、CO2发生反应时,由于要消耗H2O,引起少量NaCl晶体析出从而混入NaHCO3中,当加热NaHCO3时,NaCl不会消失而形成杂质。
(2)根据甲测定原理,样品中的Na2CO3与盐酸反应产生CO2、H2O,根据装置C中质量增加得出CO2质量,从而得到Na2CO3质量,继而得到Na2CO3质量分数,但由于空气中中的CO2、H2O会进入装置C中引起误差,利用装置D可阻止空气的CO2、H2O进入装置C而减少实验误差。根据乙方案测定原理,是利用中和滴定原理来测定Na2CO3含量的,准确称取样品后,需用1000mL 容量瓶、烧杯、玻璃棒、胶头滴管仪器将样品配制成溶液。由于样品溶液呈碱性,所以需用碱式滴定管来盛装。丙方案是根据样品中的Na2CO3与盐酸充分反后残留固体的质量来确定Na2CO3含量。甲方案中碱石灰吸收的CO2质量为3.52g,可得Na2CO3质量为=0.08mol×106g/mol=8.48g,Na2CO3质量分数=84.8%<92%,测定结果偏低,说明装置中的CO2没有被碱石灰完全吸收。乙方案中,n(Na2CO3)=![]() =0.09mol,Na2CO3的质量=0.09mol×106g/mol=9.54g,质量分数为9.54%,92%<9.54%<96%,符合误差范围。丙方案中,设10.00g 样品中含有Na2CO3的质量为x g,根据反应:Na2CO3 + 2HCl =2NaCl + CO2↑ + H2O,最后得到NaCl的质量=
=0.09mol,Na2CO3的质量=0.09mol×106g/mol=9.54g,质量分数为9.54%,92%<9.54%<96%,符合误差范围。丙方案中,设10.00g 样品中含有Na2CO3的质量为x g,根据反应:Na2CO3 + 2HCl =2NaCl + CO2↑ + H2O,最后得到NaCl的质量=![]() ,则有:10.00-x +
,则有:10.00-x +![]() =10.99,解得x=9.54g,Na2CO3质量分数为9.54%,92%<9.54%<96%,符合误差范围。
=10.99,解得x=9.54g,Na2CO3质量分数为9.54%,92%<9.54%<96%,符合误差范围。


科目:高中化学 来源: 题型:阅读理解
 (2011?天河区一模)如何降低大气中CO2的含量及有效地开发利用CO2,已受到各国的普遍重视.
(2011?天河区一模)如何降低大气中CO2的含量及有效地开发利用CO2,已受到各国的普遍重视.| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
 HCO3-+OH-
HCO3-+OH- HCO3-+OH-
HCO3-+OH- Ca2+(aq)+CO32-(aq),加入在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,溶液中c(CO32-)增大,平衡向逆方向移动
Ca2+(aq)+CO32-(aq),加入在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,溶液中c(CO32-)增大,平衡向逆方向移动 Ca2+(aq)+CO32-(aq),加入在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,溶液中c(CO32-)增大,平衡向逆方向移动
Ca2+(aq)+CO32-(aq),加入在碳酸钙饱和溶液中滴加饱和碳酸钠溶液,溶液中c(CO32-)增大,平衡向逆方向移动查看答案和解析>>
科目:高中化学 来源: 题型:

(1)碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________ (填标号)。
A.碳酸氢钠难溶于水?
B.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出?
C.碳酸氢钠受热易分解?
(2)某探究活动小组根据工业制取碳酸钠的原理,进行碳酸氢钠的制备实验, 同学们按各自设计的方案实验。?
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出)。?
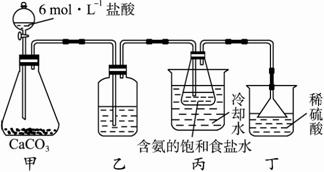
i.乙装置中的试剂是_______________(填标号)。?
A.烧碱溶液?
B.澄清石灰水?
C.浓氨水?
D.蒸馏水?
ii.丁装置的作用是_________________________。?
iii.实验结束后,分离出NaHCO3晶体的操作是_________________(填名称)。
②另一位同学用下图中戊装置(其他装置未画出)进行实验。
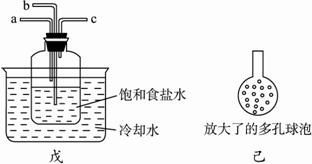
i.实验时,须先从a管通入_________气体,再从b管通入____________气体。?
ii.有同学建议在b管下端连接上图中己装置,理由是__________________________。?
(3)请你再写出一种实验室制取少量碳酸氢钠的方法。____________________________。
查看答案和解析>>
科目:高中化学 来源:2011年广东省广州市天河区高考化学一模试卷(解析版) 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com