
【题目】下列元素的单质中,最易跟氢气反应生成氢化物的是( )
A. 硼 B. 氮 C. 氟 D. 碳
科目:高中化学 来源: 题型:
【题目】下列有机反应类型判断错误的是:
A. ClCH2CH2Cl+2CH3NH2→CH3NHCH2CH2NHCH3+2HCl 取代反应
B. 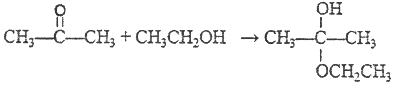 加成反应
加成反应
C. HOCH2CH2CH2OH![]()
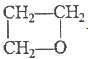 +H2O消去反应
+H2O消去反应
D. nCH2=O![]()
![]() 加聚反应
加聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 汽油、煤油和甘油的主要成分均为烃类
B. 花生油的主要成分是酯类,属于高分子化合物
C. 植物油氢化过程中发生了加成反应
D. 蛋白质是仅由碳、氢、氧元素组成的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关乙烯的说法中不正确的是( )
A. 乙烯分子中所有原子共平面
B. 乙烯使酸性高锰酸钾溶液褪色属于氧化反应
C. 乙烯使溴水褪色属于取代反应
D. 可以燃烧法鉴别甲烷和乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①能量越低的物质就越稳定;②白磷转化成红磷是放热反应。据此,下列判断或说法中正确的是
A. 在相同的条件下,红磷比白磷稳定
B. 在相同的条件下,白磷比红磷稳定
C. 红磷和白磷的结构相同
D. 红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下某溶液中由水电离出的离子浓度符合c(H+)c(OH-)=1×10-20的溶液,其pH为_________,此时水的电离受到________________。
(2)在某温度下,H2O的离子积常数为1×10-13,则该温度下:
①0.01molL-1NaOH溶液的pH=_________;
②100mL0.1molL-1H2SO4溶液与100mL0.4molL-1的KOH溶液混合后,pH=_________。
(3)已知一溶液有4种离子:X+、Y-、H+、OH-,下列分析结果肯定错误的是_________。
A.c(Y-)>c(X+)>c(H+)>c(OH-) B.c(X+)>c(Y-)>c(OH-)>c(H+)
C.c(H+)>c(Y-)>c(X+)>c(OH-) D.c(OH-)>c(X+)>c(H+)>c(Y-)
(4)在25℃下,将amolL-1的氨水与0.01molL-1的盐酸等体积混合,反应时溶液中c(NH4+)=c(Cl-)。则溶液显_________(填“酸”“碱”或“中”)性;用含a的代数式表示NH3H2O的电离常数Kb=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列溶液中离子浓度关系的表示正确的是( )
A. 在0.1 mol·L-1 KHC2O4溶液中:c(K+)+c(H+)=c(HC2O![]() )+c(OH-)+c(C2O
)+c(OH-)+c(C2O![]() )
)
B. 0.1 mol·L-1的Na2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
C. 0.1 mol·L-1的NH4NO3溶液中:c(NO![]() )>c(H+)>c(NH
)>c(H+)>c(NH![]() )>c(OH-)
)>c(OH-)
D. 物质的量浓度相等的HCOOH和HCOONa溶液等体积混合后的溶液中:2c(Na+)=c(HCOO-)+c(HCOOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。
I. K2Cr2O7曾用于检测司机是否酒后驾驶:
Cr2O72-(橙色)+CH3CH2OH![]() Cr3+(绿色)+CH3COOH (未配平)
Cr3+(绿色)+CH3COOH (未配平)
(1)基态Cr 原子的价电子轨道表达式为_________________。
(2)CH3COOH分子中所含元素的电负性由大到小的顺序为___________,碳原子的轨道杂化类型为_________,所含σ键与π键的数目之比为______________________。
(3)已知Cr3+等过渡元素水合离子的颜色如下表所示:
离子 | Se3+ | Cr3+ | Fe2+ | Zn2+ |
水合离子的颜色 | 无色 | 绿色 | 浅绿色 | 无色 |
请根据原子结构推测Se3+、Zn2+的水合离子为无色的原因为_______________________。
II. ZnCl2浓溶液常用于除去金属表面的氧化物,例如与FeO反应可得Fe[Zn(OH)Cl2]2溶液。
(4) Fe[Zn(OH)Cl2]2溶液中不存在的微粒间作用力有________(填选项字母);
A.离子键 B.共价键 C.金属键 D.配位键 E.范德华力 F.氢键
溶液中[Zn(OH)Cl2]-的结构式为_____________________。
III.锌是人体必需的微量元素之一,其堆积方式如图1,晶胞结构如图2。

(5)锌的堆积方式为_________,配位数为__________________。
(6)若梓原子的半径为a pm,阿伏加德罗常数的值为NA,则锌晶体的密度为______g/㎝3 (用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中,直接采用沾有水滴的仪器,对实验结果没有影响的是( )
A.氨的喷泉实验:烧瓶
B.实验用氯酸钾固体制取氧气:试管
C.酸碱中和滴定:锥形瓶
D.酸碱中和滴定:滴定管
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com