
A、该氖原子的相对原子质量是
| ||
| B、该氖原子的摩尔质量是aNAg | ||
C、Wg该氖原子的物质的量是
| ||
D、Wg该氖原子所含质子数是
|
| 一个原子质量 | ||
1个12C原子质量×
|
| m |
| M |
| ag | ||
bg×
|
| 12a |
| b |
| Wg |
| aNAg/mol |
| W |
| aNA |
| Wg |
| ag |
| W |
| a |
| 10W |
| a |


科目:高中化学 来源: 题型:
| A、等物质的量的OH-与羟基(-OH)所含电子数相等 |
| B、11.2g铁粉与稀硝酸反应转移电子数一定为0.6mol |
| C、1L 0.5mol/LNaHCO3溶液中含有HCO3-的个数为0.5NA |
| D、常温常压下,44g CO2气体含有氧原子的个数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后的溶液中:c(Na+)>c(CH3COO-) | ||
| B、反应前溶液的物质的量浓度:m=n | ||
| C、反应后的溶液中:c(CH3COO-)+c(CH3COOH)=m mol?L-1 | ||
D、该温度下,醋酸的电离平衡常数的表达式为:Ka=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
A、升高温度,
| ||||||
| B、通入CO2,平衡向正反应方向移动 | ||||||
| C、稀释溶液,Na2CO3水解程度增大,水解平衡常数增大 | ||||||
| D、加入NaOH固体,平衡向逆反应方向移动,溶液pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
| B、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| C、蒸发结晶时不应将溶液直接蒸干 |
| D、食盐应放在滤纸上称量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
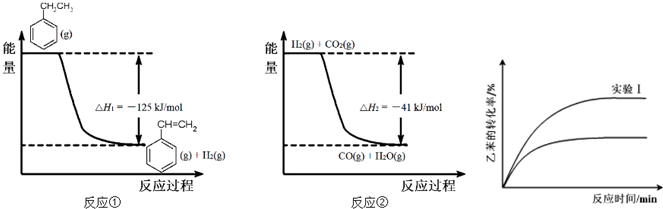
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g)的△H=
(g)+CO(g)+H2O(g)的△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验:| 试验编号 | 乙苯 | CO(g)/mol | H(g)/mol | 温度/℃ |
| Ⅰ | 3.0 | 9.0 | 0 | 550 |
| Ⅱ | 3.0 | 9.0 | 0 | 600 |
| Ⅲ | 3.0 | 0 | 9.0 | 550 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com