
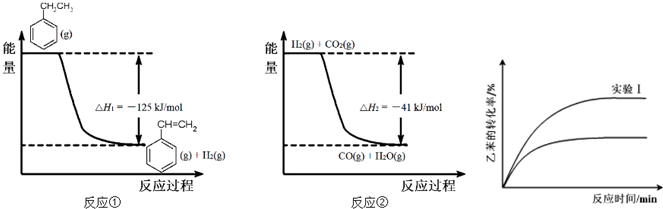
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g)的△H=
(g)+CO(g)+H2O(g)的△H= )的影响,并设计了如下实验:
)的影响,并设计了如下实验:| 试验编号 | 乙苯 | CO(g)/mol | H(g)/mol | 温度/℃ |
| Ⅰ | 3.0 | 9.0 | 0 | 550 |
| Ⅱ | 3.0 | 9.0 | 0 | 600 |
| Ⅲ | 3.0 | 0 | 9.0 | 550 |
 (g)+CO2(g)?
(g)+CO2(g)? (g)+CO(g)+H2O(g),所以该反应的反应热为:△H=△H1+△H2=-125kJ/mol-41kJ/mol=-166 kJ/mol,
(g)+CO(g)+H2O(g),所以该反应的反应热为:△H=△H1+△H2=-125kJ/mol-41kJ/mol=-166 kJ/mol,| c(苯乙烯)?c(H2) |
| c(乙苯) |
| c(苯乙烯)?c(H2) |
| c(乙苯) |
 ,通入CO2,CO2与H2反应,使c(H2)下降,平衡向正反应方向移动,乙苯的转化率提高,
,通入CO2,CO2与H2反应,使c(H2)下降,平衡向正反应方向移动,乙苯的转化率提高, ,通入CO2,CO2与H2反应,使c(H2)下降,平衡向正反应方向移动,乙苯的转化率提高.
,通入CO2,CO2与H2反应,使c(H2)下降,平衡向正反应方向移动,乙苯的转化率提高.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
A、该氖原子的相对原子质量是
| ||
| B、该氖原子的摩尔质量是aNAg | ||
C、Wg该氖原子的物质的量是
| ||
D、Wg该氖原子所含质子数是
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、产生H2体积相等 |
| B、铝产生H2最多,钠产生H2最少 |
| C、钠产生H2最多,铝产生H2最少 |
| D、钠产生H2最多,镁、铝产生H2相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
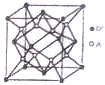 有A、B、C、D四中元素,其中A的基态原子核外电子有11中运动状态,B的基态原子得一个电子喉3p轨道就处于全充满状态,C的最常见气态氢化物呈碱性,D与A能形成离子化合物A2D且D2-比A+多一个电子层.
有A、B、C、D四中元素,其中A的基态原子核外电子有11中运动状态,B的基态原子得一个电子喉3p轨道就处于全充满状态,C的最常见气态氢化物呈碱性,D与A能形成离子化合物A2D且D2-比A+多一个电子层.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
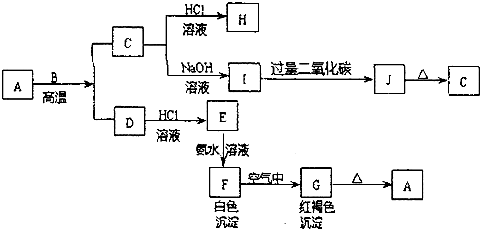
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com