
科目:高中化学 来源:2014-2015江西省宜春市高二下学期第一次月考化学试卷(解析版) 题型:选择题
某有机物A是农药生产中的一种中间体,其结构简式如下图。则下列叙述正确的是
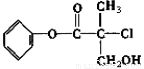
A.有机物A分子式为C10H12O3Cl
B.有机物A可以和Br2的CCl4溶液发生加成反应
C.有机物A和浓硫酸混合加热,可以发生消去反应
D.1molA和足量的NaOH溶液反应,最多可以消耗3mol NaOH
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省台州市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列有关键线式的说法中错误的是:
A.将碳、氢元素符号省略,只表示分子中键的连接情况
B.每个拐点、交点、端点均表示有一个碳原子
C.每一条线段代表一个共价键,每个碳原子有四条线段,用四减去线段数即是氢原子数
D.C=C、C≡C键等官能团中的“=”和“≡”也可以省略
查看答案和解析>>
科目:高中化学 来源:2014-2015四川省达州市高一3月月考化学试卷(解析版) 题型:选择题
CO2的资源化利用是解决温室效应的重要途径。以下是在一定条件下用NH3捕获CO2生成重要化工产品三聚氰胺的反应:NH3+CO2→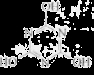 +H2O,下列有关三聚氰胺的说法正确的是
+H2O,下列有关三聚氰胺的说法正确的是
A.分子式为C3H6N3O3
B.属于共价化合物
C.分子中既含极性键,又含非极性键
D.生成该物质的上述反应为中和反应
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:实验题
(10分)某同学做同周期 元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:
实验方案 | 实验现象 |
①用砂纸擦后的镁带与沸水反应,再向反应后溶液中滴加酚酞 | (a)浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
②向新制的H2S饱和溶液中滴加新制的氯水 | (b)产生气体,可在空气中燃烧,溶液变成浅红色 |
③钠与滴有酚酞试液的冷水反应 | (c)反应不十分强烈,产生无色气体 |
④镁带与2 mol·L-1的盐酸反应 | (d)剧烈反应,产生无色气体 |
⑤铝条与2 mol·L-1的盐酸反应 | (e)生成白色胶状沉淀,既而沉淀消失 |
⑥向AlCl3溶液中滴加NaOH溶液至过量 | (f)生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告:
(1)实验目的:____________________________________________________________。
(2)实验用品:仪器:试管、酒精灯、砂纸、镊子、小刀、胶头滴管、滤纸
药品:镁带、钠、铝条、新制氯水、新制饱和硫化氢溶液、2 mol·L-1的盐酸、NaOH溶液、蒸馏水、酚酞、AlCl3溶液
(3)实验内容:(填写题给信息表中的序号)
实验方案 | 实验现象(填写序号) |
① | |
② | |
③ | |
④ | |
⑤ | |
⑥ |
实验结论:__________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
aXn-和bYm+为两主族元素的离子, 它们的电子层结构相同, 下列判断错误的是
A.原子半径X<Y B.a+n=b-m
C.离子半径X n-<Y m+ D.X的氢化物的化学式为HnX
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省高一下学期第一次月考化学试卷(解析版) 题型:选择题
关于化学键的下列叙述中,正确的是
A.离子化合物中可能含离 子键 B.共价化合物中可能含离子键
子键 B.共价化合物中可能含离子键
C.离子化合物中不含共价键 D.共价化合物中不含离子键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年重庆市西北狼教育联盟高三第二次联合考试理综化学试卷(解析版) 题型:填空题
(16分)(一)在温度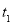 和
和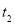 下,卤素X2(g)和H2反应生成HX的平衡常数如下表:
下,卤素X2(g)和H2反应生成HX的平衡常数如下表:
化学方程式 | K(t1) | K(t2) |
F2+H2 | 1.8×1036 | 1.9×1032 |
Cl2+H2 | 9.7×1012 | 4.2×1011 |
Br2+H2 | 5.6×107 | 9.3×106 |
I2+H2 | 43 | 34 |
(1)已知t2>t1,生成HX的反应是 反应(填“吸热”或“放热”)。
(2)用电子式表示HCl的形成过程 。
(3)共价键的极性随共用电子对偏移程度的增大而增强,HX共价键的极性由强到弱的顺序是 (用化学式表示)。
(4)K的变化体现出X2化学性质的递变性,用原子结构解释原因是 。
(二)下图表示一些晶体结构,它们分别是晶体干冰、金刚石、氯化铯、氯化钠某一种的某一部分。
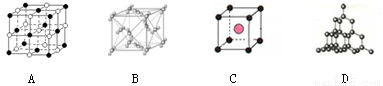
(5)代表金刚石的是 (选填字母);晶体中碳原子与C—C键数目之比是 。
(6)上述B、C、D三种物质熔点由高到低的排列顺序为 (用字母表示)。
(7)金属镍及其化合物在合金材料以及催化剂等方面应用广泛,NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69pm和78pm,则熔点NiO FeO(填“<,>或=”)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年贵州省八校联盟高三第二次联考理综化学试卷(解析版) 题型:选择题
某课外兴趣小组进行电解原理的实验探究,做了如下的实验:以铜为电极,按如图所示的装置电解饱和食盐水。
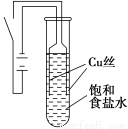
实验现象:接通电源30 s内,阳极附近出现白色浑浊,之后变成橙黄色浑浊,此时测定溶液的pH约为10。一段时间后,试管底部聚集大量红色沉淀,溶液仍为无色。
查阅资料:
物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜(不稳定) | 氯化亚铜 |
颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
*相同温度下CuCl的溶解度大于CuOH
下列说法错误的是
A.反应结束后最终溶液呈碱性
B.阴极上发生的电极反应为:2H2O + 2e- ═ H2↑+ 2OH-
C.电解过程中氯离子移向阳极
D.试管底部红色的固体具有还原性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com