
【题目】按要求完成下列填空:
(1)![]() 、
、![]() 、
、![]() 互为______,16O2、18O3互为______。
互为______,16O2、18O3互为______。
A.同位素 B.相同物质
C.同素异形体 D.同分异构体
(2)写出下列物质的电子式:
①MgCl2______;②NaOH______;
(3)写出下列物质的结构式:
①C2H2_______;②H2O________;
(4)已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为______________________。
【答案】 A C ![]()
![]() H—C≡C—H H—O—H N2(g)+3H2(g)
H—C≡C—H H—O—H N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92kJ/mol(不写可逆符号不扣分)
2NH3(g) ΔH=-92kJ/mol(不写可逆符号不扣分)
【解析】本题分析:本题主要考查基本概念。
(1)![]() 、
、![]() 、
、![]() 是质子数相同、子数不同的原子,互为同位素,故选A,16O2、18O3是氧元素的不同单质,互为同素异形体,故选C。
是质子数相同、子数不同的原子,互为同位素,故选A,16O2、18O3是氧元素的不同单质,互为同素异形体,故选C。
(2)①MgCl2是离子化合物,用阴阳离子的电子式表示:![]() ;②NaOH是离子化合物,用阴阳离子的电子式表示:
;②NaOH是离子化合物,用阴阳离子的电子式表示:![]() 。
。
(3)①C2H2的结构式:H—C≡C—H;②H2O的结构式:H—O—H;
(4)△H =拆键消耗能量-成键释放能量=(3×436+946-2×3×391) kJ/mol=-92kJ/mol,则N2与H2反应生成NH3的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92kJ/mol。
2NH3(g) ΔH=-92kJ/mol。


科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为____________。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:_____________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) ===H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为______________kJ。
(4)Bodensteins研究了下列反应:
2HI(g)![]() H2(g) + I2(g)
H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
① 根据上述实验结果,该反应的平衡常数K的计算式为:___________。
② 上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为________(以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=__________min-1
③ 由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_________________(填字母)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W用作调香剂、高分子材料合成的中间体等,制备W的一种合成路线如下。
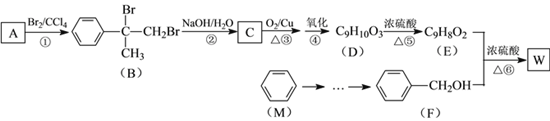
已知:![]()
请回答下列问题:
(1)F的化学名称是_________,②的反应类型是_________。
(2)D中含有的官能团是________________(写名称),D聚合生成高分子化合物的结构简式为_____________。
(3)反应③的化学方程式是______________________。
(4)反应⑥的化学方程式是______________________。
(5)芳香化合物N是A的同分异构体,其中核磁共振氢谱为三组峰的结构简式为
_______________。
(6)参照有机物W的上述合成路线,设计以M为起始原料制备F的合成路线(无机试剂任选)。[示例:![]() ]
]
____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2 L的密闭容器中,加入1 mol X(g)和2 mol Y(g)发生反应:X(g)+mY(g)![]() 3Z(g)平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、 Z的体积分数不变。下列叙述不正确的是( )
3Z(g)平衡时, X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1mol Z(g),再次达到平衡后,X、Y、 Z的体积分数不变。下列叙述不正确的是( )
A.m=2 B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为 1∶1 D.第二次平衡时,Z的浓度为 0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,我国重点城市空气质量日报的监测项目中不包括
A.二氧化硫(SO2) B.二氧化碳(CO2)
C.二氧化氮(NO2) D.总悬浮颗粒物(TSP)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各组物质中,分子数一定相同的是 ( )
A.0.2mol H2和4.48L HCl气体
B.标准状况下1mol O2和22.4L H2O
C.4g 氦气和标准状况下22.4LCO2
D.4L CO和4L CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备气体常用的装置图,请回答下面相关问题:
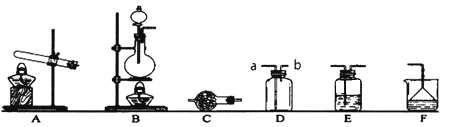
(1)某同学若选取A装置制备氨气。
①A装置制备氨气的化学方程式为______________________________________。
②某同学用氨气和滴加酚酞的水做喷泉实验,根据烧瓶内产生红色喷泉的现象,说明氨气具有___________性质(填序号)。
a.还原性 b.氧化性 c.极易溶于水 d.与水反应生成碱性物质
③干燥氨气时,常常在装置C中加入________________作干燥剂。
④如图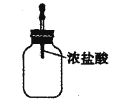 在收集满氨气的集气瓶中,挤压装置中的胶头滴管,滴入1~2 滴浓盐酸,可观察到的现象是_______________________________。
在收集满氨气的集气瓶中,挤压装置中的胶头滴管,滴入1~2 滴浓盐酸,可观察到的现象是_______________________________。
(2)某同学选取B装置为探究铜跟浓硫酸的反应情况。
①写出B装置中所发生反应的化学方程式___________________________________
②下列药品中能够用来验证反应停止后的烧瓶中有H2SO4剩余的是__________(填字母编号)。
a.BaCl2溶液 b.NaHCO3粉末 c.Ba(NO3)2溶液 d.银粉
③若采用D装置收集气体,则进气管应该接______(填写“a”或“b”),多余的气体需要通过F装置吸收,F装置所装的溶液是________,F装置中倒置的漏斗作用是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知还原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如下实验:
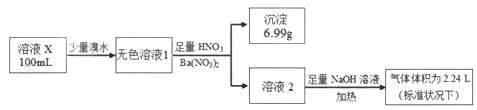
下列说法正确的是
A. 溶液X肯定只存在NH4+、SO42-
B. 溶液X一定不含有Ba2+、Fe3+,可能含有I-
C. 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液
D. 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com