
【题目】下列各组物质中,X 表示某物质,Y 表示 X 物质中含有的少量杂质,Z 表示要除去杂质加入的试剂,其中正确的组别是

A. AB. BC. CD. D
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】Atropic 酸(H)是某些具有消炎、镇痛作用药物的中间体,其一种合成路线如下:
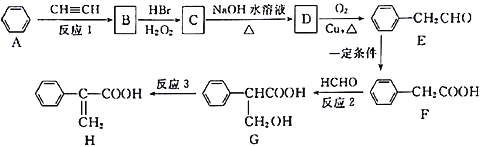
(1)G中含氧官能团的名称是____________;反应1为加成反应,则B的结构简式是________________。
(2)反应2的反应类型为________________,反应3的反应条件为________________。
(3)C→D的化学方程式是________________________________。
(4)写出E与银氨溶液水浴反应的离子方程式_______________________________。
(5)下列说法正确的是________。
a. B中所有原子可能在同一平面上
b. 合成路线中所涉及的有机物均为芳香族化合物
c.一定条件下1mol有机物H最多能与5molH2发生反应
d. G能发生取代、加成、消去、氧化、缩聚等反应
(6)化合物G有多种同分异构体,其中同时满足下列条件:①能发生水解反应和银镜反应; ②能与FeC13发生显色反应;③核磁共振氢谱只有4个吸收峰的同分异构体的结构简式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行下列实验,现象和结论均正确的是
选项 | ① | ② | ③中现象 | 结论 | 装置图 |
A | 浓硝酸 | Cu | 淀粉-KI溶液变蓝 | NO2为氧化性气体 |
|
B | 稀硫酸 | Na2SO3 | 品红溶液褪色 | Na2SO3未变质 | |
C | 浓盐酸 | MnO2 | FeBr2溶液变为黄色 | 氧化性:Cl2>Br2 | |
D | 浓氨水 | NaOH | 湿润红色石蕊试纸变蓝 | NH3为碱性气体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近日,中国科学家研发了一种碳修饰的镍基催化剂,实现了木质素选择性氢解得到酚类化合物。请回答下列问题:
(1)基态碳原子的核外电子有____种运动状态, 基态Ni原子的核外电子排布式为_________________。
(2)C、N、O三种元素的第一电离能由大到小的顺序为______________________。
(3)图1所示化合物中碳原子的杂化方式为_________,存在的化学键类型有_________(填标号)。

A.共价键 B.离子键 C.配位键 D.金属键 E.氢键
(4)碳的氧化物CO常作为许多金属配合物的配体,CO与N2互为等电子体,则CO分子中σ键与π键的个数比为______;测得熔点为170℃,预测属于___________晶体。
(5)一种储氢材料由镍、 镁元素组成,其晶胞结构如图2所示,则该晶体的化学式为__________,其晶胞边长为apm,列式计算晶胞密度为___________g/cm3 (不必计算出结果,阿伏加德岁常数的值为NA)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA 代表阿伏加德罗常数的值,下列说法正确的是( )
A. 1mol O2 作为氧化剂参与反应,得到的电子数一定为 4NA
B. 1mol Fe 和足量稀硫酸反应,失去的电子数是 3NA
C. 0.4mol·L-1Na2SO4 溶液中,所含 Na+和SO42- 总数为 1.2NA
D. 标准状况下,23g Na 所占的体积一定小于 22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是短周期主族元素,且原子序数依次增大。在短周期中A元素原子半径最小,D元素原子半径最大,B的简单氢化物的水溶液呈碱性,C、E同主族,形成的化合物为EC2、EC3。回答下列问题:
(1)E在元素周期表中的位置为__________。
(2)D2E溶液在空气中长期放置发生反应,生成物之一为H。H与Na2O2的结构和化学性质相似,其溶液显黄色。H的电子式为______。
(3)化学家发现一种化学式为A4B4的化合物,由均带一个电荷的阴、阳离子组成,则该阴、阳离子为_______。
(4)B2A4C3是一种常见的炸药,其在常温下撞击时会生成一种气体(B2C)和一种常见液体,该反应的化学力程式为______________。8g该物质反应转移的电子数目为________。
(5)下列事实能说明元素F的非金属性比元素E的非金属性强的是______。
a.元素F形成的单质比元素E形成的单质的熔点低
b.F和E两元素的简单氢化物受热分解,前者的分解温度高
c.F2通入到D2E的溶液中出现浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298K、1.01×105Pa,O2、S、Se、Te分别与H2化合的反应热数据如图所示。写出Se与H2化合的热化学反应方程式正确的是

A. Se(s)+ H2(g) = H2Se(g) ΔH=-242kJ·mol-1
B. Se(s)+ H2(g) = H2Se(g) ΔH=-20kJ·mol-1
C. Se(g)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
D. Se(s)+ H2(g) = H2Se(g) ΔH=+81kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 ②Na2CO3溶液和NaHCO3溶液都能跟盐酸反应 ③钠在常温下不容易被氧化 ④Na2O2可作供氧剂,而Na2O不行
A. 都正确 B. ②③④ C. ②③ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电。
①该电池负极的电极反应式为__________________。
②若以该电池为电源,用石墨作电极电解200 mL含有如下离子的溶液。
离子 | Cu2+ | H+ | Cl | SO42- |
c/mol·L-1 | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件下)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为____。
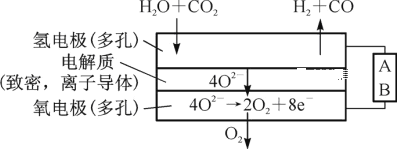
(2)电解水蒸气和CO2产生合成气(H2+CO)。较高温度下(700~1 000℃),在SOEC两侧电极上施加一定的直流电压,H2O和CO2在氢电极发生还原反应产生O2—,O2—穿过致密的固体氧化物电解质层到达氧电极,在氧电极发生氧化反应得到纯O2。由图可知A为直流电源的____(填“正极”或“负极”),请写出以H2O为原料生成H2的电极反应式:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com