
已知常温下,在溶液中发生如下反应:① 16H++10Z-+2XO4-=2X2++5Z2+8H2O;
②2A2++B2=2A3++2B-; ③2B-+Z2=B2+2Z-由此推断下列说法错误的是
A. 反应2A3++2Z-= Z2+2A2+可以进行
B. Z元素在①反应中被氧化,在③反应中被还原
C. 还原性由强到弱的顺序是A2+,B-,Z-,X2+
D. 氧化性由强到弱的顺序是XO4-,Z2,B2,A3+
科目:高中化学 来源: 题型:
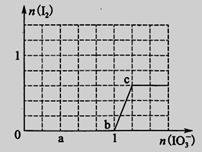
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,试回答下列问题:
(1)写出a点反应的离子方程式________________;反应中还原剂是______________;被还原的元素是__。
(2)写出b点到c点反应的离子方程式_____________________________。
(3)若往100 mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中发生反应N2+3H2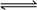 2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
2NH3 , ΔH<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:
回答下列问题:
(1)处于平衡状态的时间段是__________(填选项)。
A.t0~t1 B.t1~t2 C.t2~t3
D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项),t1时刻________; t4时刻________。
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是__________(填选项)。
A.t0~t1 B.t2~t3 C. t3~t4 D.t5~t6
(4)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将下列各组物质按单质、酸、碱、盐分类顺序排列,其中正确的是
A.水银、硫酸、烧碱、硫酸氢钠 B.碘酒、盐酸、烧碱、硫酸钡
C.氧气、硝酸、纯碱、胆矾 D.铁、醋酸、碱式碳酸铜、氯化铜
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在指定条件下能大量共存的是
A.氢氧化铁胶体中: H+、Cu2+、Cl-、NO3-
B.pH=1的溶液中:Na+、CH3COO﹣、Cl﹣、Cu2+
C.使紫色石蕊试液变蓝的溶液中:K+、Cl-、NO3-、HCO3-
D.澄清透明溶液中:Cu2+、K+、NO3﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
“探险队员”——盐酸,不小心走进了化学迷宫,迷宫有许多“吃人的野兽”(即能与盐酸反应的物质),盐酸必须避开它们,否则就无法通过。
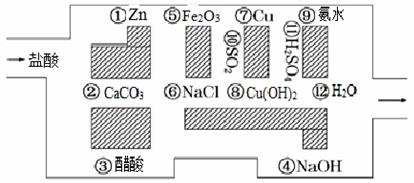
(1)请你帮助它走出迷宫(用图中物质前的序号连接起来表示所走的路线)___________。
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有__________个,属于氧化还原反应的有__________个。
(3)在不能与盐酸反应的物质中,属于非电解质的是________(填写物质序号),在能与盐酸反应的物质中,属于强电解质的是__________(填写物质序号)。
(4)写出物质②的电离方程式
(5)如果将盐酸换成氯化钡,它能沿着盐酸走出的路线“走出”这个迷宫吗?
填“能”或“不能”_____,若不能请写出离子方程式说明其原因:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在 5L密闭容器中进行,30秒后,NO的物质的量增加了0.3 mol,则此反应的平均速率v(x)(表示反应物的消耗速率或生成物的生成速率)为( )
A.v (O2)= 0.0l mol·L-1·s-1 B.v (NO)=0.001 mol·L-1·s-1
C. v (NH3)=0.001 mol·L-1·s-1 D. v (H2O)=0.003 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知有一种节能的氯碱工业新工艺,将电解池和燃料电池相组合,相关流程如下图所示(电极未标出):回答下列有关问题:
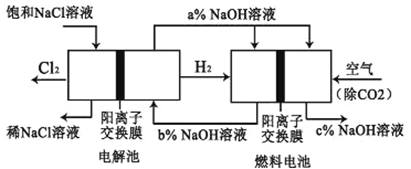
(1)燃料电池的正极反应式为 ________ _▲ ____ _;
燃料电池中阳离子的移动方向_______▲____(“从左向右”或“从右向左”)。
(2)电解池中阳离子交换膜的作用(写出两点) ▲
(3)电解池中产生2 mol Cl2,理论上燃料电池中消耗__▲___ mol O2。
(4)a、b、c的大小关系为:_____▲_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
为检验某卤代烃(R—X)中的X元素,有下列实验操作:①加热煮沸 ②加入AgNO3溶液 ③取少量的卤代烃 ④加入稀硝酸酸化 ⑤加入NaOH溶液 ⑥冷却。正确操作的先后顺序是( )
A.③①⑤⑥②④ B.③②①⑥④⑤ C.③⑤①⑥④② D.③⑤①⑥②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com