
【题目】[化学—选修5:有机化学基础]
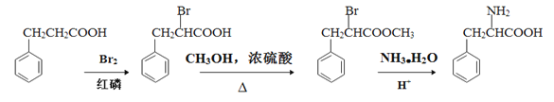
利用化学方法合成味精的路线如下图所示:
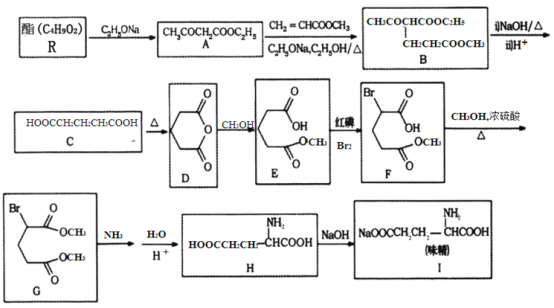
请回答以下问题:
(1)R的结构简式为________;由A生成B的反应类型是________。
(2)F中含氧官能团的名称为________;化合物H的化学名称为________________。
(3)写出由C生成D的化学方程式________________。
(4)写出一种符合下列要求的A的同分异构体的结构简式________。
①结构中含有六元环,光谱测定显示,分子结构中不存在甲基;
②能在NaOH溶液中发生水解反应;
③1mol该物质与足量金属Na反应能够生成0.5mol H2
(5)参照上述合成路线,写出以苯丙酸(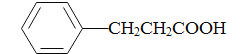 )和甲醇(其它无机试剂任选),设计合成苯丙氨酸(
)和甲醇(其它无机试剂任选),设计合成苯丙氨酸(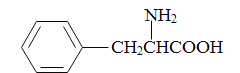 )的路线。_______________________________________________________________________
)的路线。_______________________________________________________________________
【答案】CH3COOCH2CH3 加成反应 羧基、酯基 2-氨基-1,5-戊二醇或![]() -氨基-1,5-戊二醇 HOOCCH2CH2CH2COOH
-氨基-1,5-戊二醇 HOOCCH2CH2CH2COOH![]()
![]() +H2O
+H2O 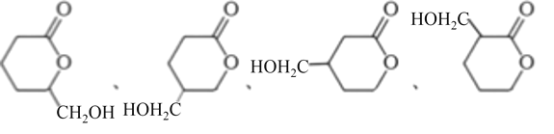
【解析】
(1)根据R的分子式和生成的A的结构简式以及反应条件判断R的结构简式;A到B反应物丙烯酸甲酯的双键被加成;
(2)F中含氧官能团为羧基和酯基;根据系统命名法命名H;
(3)根据D的结构可知C中的两个羧基一个脱掉羟基一个脱掉氢反应生成环。
(4)能在NaOH溶液中发生水解反应说明含有酯基;③1mol该物质与足量金属Na反应能够生成0.5mol H2说明还含有1个-OH;
(5)![]() 与Br2/红磷作用得到
与Br2/红磷作用得到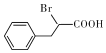 ,再与甲醇发生酯化反应生成
,再与甲醇发生酯化反应生成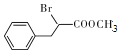 ,最后经过①NH3、②H2O/H+得到
,最后经过①NH3、②H2O/H+得到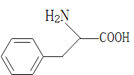 。
。
(1)R的分子式为C4H8O2且为酯类即含有酯基,和C2H5ONa反应后生成A ![]() ,反推可知R为:CH3COOCH2CH3;A到B反应物丙烯酸甲酯的双键被加成,反应类型为加成反应;
,反推可知R为:CH3COOCH2CH3;A到B反应物丙烯酸甲酯的双键被加成,反应类型为加成反应;
故答案为:CH3COOCH2CH3;加成反应
(2)F中含氧官能团为羧基和酯基;根据系统命名法可知H的名称为:2-氨基-1,5-戊二醇或![]() -氨基-1,5-戊二醇
-氨基-1,5-戊二醇
故答案为:羧基、酯基;2-氨基-1,5-戊二醇或![]() -氨基-1,5-戊二醇;
-氨基-1,5-戊二醇;
(3)根据D的结构可知C中的两个羧基一个脱掉羟基一个脱掉氢发生反应,
故答案为:HOOCCH2CH2CH2COOH![]()
![]() +H2O;
+H2O;
(4)A的分子式为C5H10O3,其同分异构体结构中含有六元环,光谱测定显示,分子结构中不存在甲基,含有酯基,还含有1个-OH,符合要求的同分异构体有
 ;
;
(5)![]() 与Br2/红磷作用得到
与Br2/红磷作用得到![]() ,再与甲醇发生酯化反应生成
,再与甲醇发生酯化反应生成 ,最后经过①NH3、②H2O/H+得到
,最后经过①NH3、②H2O/H+得到 ,合成路线流程图为:
,合成路线流程图为: 。
。


 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
【题目】夏日的夜晚,常看到儿童手持荧光棒嬉戏,荧光棒发光原理是利用![]() 氧化草酸二酯(
氧化草酸二酯(![]() )产生能量,该能量被传递给荧光物质后发出荧光。草酸二酯的结构简式如图所示,下列有关草酸二酯的说法不正确的是( )
)产生能量,该能量被传递给荧光物质后发出荧光。草酸二酯的结构简式如图所示,下列有关草酸二酯的说法不正确的是( )
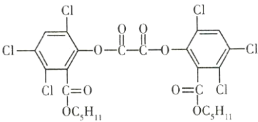
A.1mo草酸二酯与![]() 完全加成,需要消耗6mol
完全加成,需要消耗6mol![]()
B.草酸二酯的分子式为![]()
C.草酸二酯能发生取代反应
D.1mol草酸二酯最多可与4mol![]() 反应
反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应N2O4(g)![]() 2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) △H=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )

A. a、c两点的反应速率:a>c
B. a、c两点气体的颜色:a深,c浅
C. b、c两点的转化率:b>c
D. 由b点到a点,可以用加热的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组以CoCl2·6H2O、NH4Cl、H2O2、液氨、氯化铵为原料,在活性炭催化下合成了橙黄色晶体X。为测定其组成,进行如下实验。
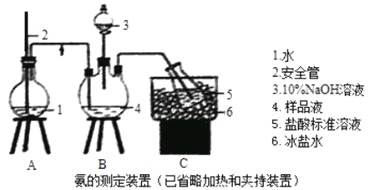
①氨的测定:精确称取wgX,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,用V1mLc1mol·L—1的盐酸溶液吸收。蒸氨结束后取下接收瓶,用c2mol·L—1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2mLNaOH溶液。
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现砖红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是_________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____式滴定管,可使用的指示剂为________。
(3)样品中氨的质量分数表达式为____________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将___(填“偏高”或“偏低”)。
(5)测定氯的过程中,使用棕色滴定管的原因是___________;滴定终点时,若溶液中c(Ag+)=2.0×10—5mol·L—1,c(CrO42—)为______mol·L—1。(已知:Ksp(Ag2CrO4)=1.12×10—12)
(6)经测定,样品X中钴、氨、氯的物质的量之比为1:6:3,钴的化合价为______,制备X的化学方程式为____________________;X的制备过程中温度不能过高的原因是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锗是一种重要的战略资源,在半导体、航空航天测控等领域都有着广泛的应用。下图是以一种锗矿![]() 主要成分为
主要成分为![]() 、
、![]() 、
、![]() 为原料制备锗的工艺流程:
为原料制备锗的工艺流程:
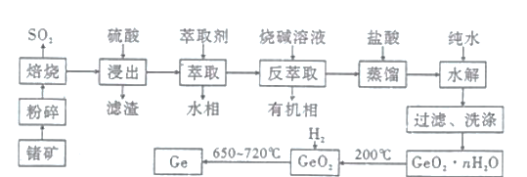
已知:
![]() 为两性氧化物。
为两性氧化物。
![]() “萃取”时用的萃取剂在本实验条件下对
“萃取”时用的萃取剂在本实验条件下对![]() 有很好的选择性。
有很好的选择性。
![]() 的熔、沸点分别为
的熔、沸点分别为![]() 、
、![]() ,极易水解放热。
,极易水解放热。
![]() “蒸馏”过程中发生的反应为
“蒸馏”过程中发生的反应为![]() 。
。
(1)锗在元素周期表中的位置为第_________周期第________族。
(2)“粉碎”的目的是_______________________。
(3)“焙烧”过程中![]() 发生反应的化学方程式为________________。
发生反应的化学方程式为________________。
(4)“滤渣”的成分为________________![]() 填化学式
填化学式![]() ,“水相”中的阳离子除了
,“水相”中的阳离子除了![]() 和
和![]() 外,还有__________________
外,还有__________________![]() 填离子符号
填离子符号![]() 。
。
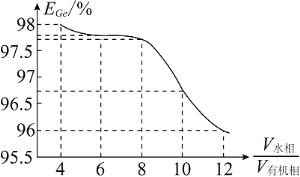
(5)“萃取”时,![]() 锗的萃取率
锗的萃取率![]() 与
与![]() 水相与有机相的体积比
水相与有机相的体积比![]() 的关系如图所示,从生产成本的角度考虑,最适宜的
的关系如图所示,从生产成本的角度考虑,最适宜的![]() 为______________
为______________![]() 填序号
填序号![]() 。
。
![]()
![]()
![]()
![]()
(6)“水解”时反应的化学方程式为_________________,该步实验操作必须在冰盐浴中进行的原因除了有利于水解反应正向进行外,还有______________。
(7)假设流程中每步都没有锗元素损失,若![]() 锗
锗 ![]() 含锗
含锗![]() 经提纯得到
经提纯得到![]() 的锗,则杂质元素的脱除率为_____________
的锗,则杂质元素的脱除率为_____________![]() 用含a、b、c的式子表示
用含a、b、c的式子表示![]() 。
。![]() 已知:杂质元素的脱除率
已知:杂质元素的脱除率![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为![]() )提取氧化铝作冶炼铝的原料,提取的操作过程如下:
)提取氧化铝作冶炼铝的原料,提取的操作过程如下:

(1)反应1结束后的操作名称为_______。
(2)滤渣的主要成分是___________________。
(3)反应2中通入的过量气体为________
a. 二氧化碳 b.氨气 c.氮气
(4)写出B煅烧生成Al2O3的化学反应方程式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铋及其化合物在工业生产中用途广泛,某研究小组用浮选过的辉铋矿![]() 主要成分是
主要成分是![]() ,还含少量
,还含少量![]() 等杂质
等杂质![]() 制备
制备![]() ,其流程如下:
,其流程如下:

已知:![]() 水解能力:
水解能力:![]()
![]() 。
。
回答下列问题:
(1)“浸取”时,为了提高浸取速率,可采取的措施有___________![]() 任写一条
任写一条![]() ;过滤1的滤渣的主要成分有______________
;过滤1的滤渣的主要成分有______________![]() 填化学式
填化学式![]() 。
。
(2)浸取时加入过量浓盐酸的目的是____________________________________。
(3)写出焙烧时生成铋酸钠的化学方程式_________________________________。
(4)![]() 时,向浓度均为
时,向浓度均为![]() 的
的![]() 、
、![]() 的混合溶液中滴加
的混合溶液中滴加![]() 溶液
溶液![]() 设溶液体积增加1倍
设溶液体积增加1倍![]() ,当
,当![]() 时恰好完全沉淀,判断此时
时恰好完全沉淀,判断此时![]() 是否已经开始沉淀________
是否已经开始沉淀________![]() 填“是”或“否”
填“是”或“否”![]() 已知:
已知:![]() 、
、![]()
(5)用双硫腙![]() ,二元弱酸
,二元弱酸![]() 络合萃取法可从工业废水中提取金属离子:
络合萃取法可从工业废水中提取金属离子:![]() 先将金属离子络合成电中性的物质
先将金属离子络合成电中性的物质![]() 如
如![]() 等
等![]() ,再用
,再用![]() 萃取此络合物。下图是用上述方法处理含有
萃取此络合物。下图是用上述方法处理含有![]() 、
、![]() 、
、![]() 的废水时的酸度曲线
的废水时的酸度曲线![]() 表示金属离子以络合物形式被萃取分离的百分率
表示金属离子以络合物形式被萃取分离的百分率![]() 。
。

![]() 当调节
当调节![]() 时,铋
时,铋![]() 的存在形式为____________。
的存在形式为____________。
![]() 向萃取后的
向萃取后的![]() 中加入过量NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为____。
中加入过量NaOH溶液可将铋元素以氢氧化物的形式沉淀下来,相应的离子方程式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期中的18种元素具有重要的用途,在现代工业中备受青睐。
(1)钛原子的价电子排布式为______________________,TiCl4沸点136℃,熔点-25℃,晶体类型为___________晶体。
(2)铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________。
(3)与As同主族的短周期元素是N、P。AsH3中心原子轨道杂化的类型_________________;一定压强下将AsH3、NH3和PH3的混合气体降温时液化顺序是______________________,理由是______________________。
(4)铬是一种硬而脆抗腐蚀性强的金属,常用于电镀和制造特种钢。下图1为铬的晶胞结构图,则铬晶胞属于___________堆积;该晶胞中原子的体积占晶胞体积的百分率为___________。

(5)钴晶体的一种晶胞(如图2所示)的边长为anm,密度为ρg·cm-3,NA表示阿伏加德罗常数的值,则钴原子半径为___________mm,钴的相对原子质量可表示为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,答下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2该反应氧化剂与还原剂物质的量之比为_______________。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
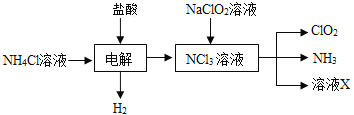
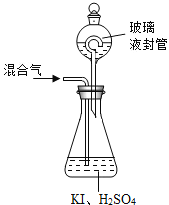
图1 图2
①电解时发生反应的化学方程式为_______________________________________________ 。
②溶液X中大量存在的阴离子有________________________________________________ 。
③除去ClO2中的NH3可选用的试剂是 ___________________(填标号)。
a.水 b.碱石灰 c.浓硫酸 d.饱和食盐水
(3)用上图2装置可以测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL 稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为_______________________________。
②玻璃液封装置的作用是________________________________________________。
③V中加入的指示剂通常为___________,滴定至终点的现象是_________________________。
④测得混合气中ClO2的质量为____________________________ g.。
(4)O2处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下列物庾最适宜的是________(填标号)。
a.明矾 b.碘化钾 c.盐酸 d.硫酸亚铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com