
【题目】下列反应中,水只作氧化剂的氧化还原反应为: ( )
A.Cl2+H2O=HCl+HClOB.2F2+2H2O=4HF+O2
C.H2O+CaO=Ca(OH)2D.2Na+2H2O=2NaOH+H2↑
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】聚合硫酸铁[Fe2(OH)n(SO4)3﹣n/2]m是一种新型高效的水处理混凝剂,某课题小组设计如下方案制备聚合硫酸铁,其简单工艺流程如图1:
为测定溶液Ⅰ中铁元素的总含量,实验操作如下:准确量取20.00mL溶液Ⅰ于带塞锥形瓶中,加入足量H2O2 , 调节pH<3,加热煮沸;加入过量KI充分反应后,再用0.1 000molL﹣1 Na2S2O3标准溶液滴定至终点,消耗标准溶液VXmL.已知:I2+2S2O32﹣═I﹣+S4O62﹣ . .
(1)实验过程中加热煮沸的目的是 .
(2)在测定过程中加入足量H2O2发生反应离子方程式: .
(3)滴定过程中选择装标准溶液仪器(如图2)是否合理(填“是”或“否”)
(4)写出滴定选用的指示剂 , 滴定终点观察到的现象 .
(5)根据图1消耗的Na2S2O3标准溶液体积,计算出溶液Ⅰ中铁元素的总含量为gL﹣1 . 若滴定前溶液中H2O2没有除尽,所测定的铁元素的含量将会(填“偏高”“偏低”或“不变”).
(6)上述流程中溶液Ⅰ中铁元素存在不同的离子,根据题意完成下面假设并设计实验方案证明假设假设1:溶液Ⅰ中只存在Fe2+ 假设2:溶液Ⅰ中只存在Fe3+ 假设3: .
根据提供试剂和实验用品验证假设3成立
限选实验试剂:1.0molL﹣1 NaOH溶液、8.0molL﹣1 NaOH溶液、0.01molL﹣1KMnO4、淀粉﹣KI溶液、3moLL﹣1H2SO4、紫色石蕊试液、0.1molL﹣1 K3[Fe(CN)6]溶液、试管、胶头滴管
实验步骤 | 预期现象和结论 |
步骤1:取少量溶液Ⅰ于试管A、B中 | |
步骤2: | |
步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:下列描述正确的是( ) 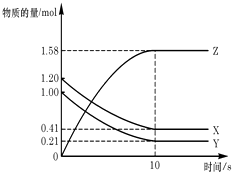
A.反应开始到10s,用Z表示的反应速率为0.158mol/(Ls)
B.反应开始到10s,X的物质的量浓度减少了0.79mol/L
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为:X(g)+Y(g)Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中进行如下反应:CO(g)+H2O(g)CO2(g)+H2(g),有如下数据:
实验 | 温度/℃ | 起始量/mol | 平衡量/mol | |||
CO | H2O | CO2 | H2 | CO2 | ||
1 | 650 | 2.0 | 1.0 | 0 | 0 | 0.8 |
2 | 800 | 2.0 | 2.0 | 0 | 0 | 1.0 |
下列说法正确的是( )
A.正反应为吸热反应
B.实验1中,CO的转化率为80%
C.650℃时,化学平衡常数K= ![]()
D.实验1再加入1.0 mol H2O,重新达到平衡时,n(CO2)为1.6 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com