
【题目】A、B、C、D四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8。A元素原子的第二层电子数与第一、第三层电子数之和相等,D元素原子的第一、第二层电子数之和等于电子总数的一半。试回答下列问题。
(1)四种元素的符号依次是A___,B___,C__,D__;它们的原子半径由大到小的顺序是___。
(2)试写出四种元素的离子结构示意图:A___,B___,C___,D___。它们的离子半径由大到小的顺序是___(用离子符号表示)。
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:__。
(4)分别写出A、B两元素的气态氢化物的化学式:__。
【答案】S Cl K Ca K>Ca>S>Cl ![]()
![]()
![]()
![]() S2->Cl->K+>Ca2+ H2SO4、HClO4、KOH、Ca(OH)2 H2S、HCl
S2->Cl->K+>Ca2+ H2SO4、HClO4、KOH、Ca(OH)2 H2S、HCl
【解析】
A元素原子的第二层电子数与第一、第三层电子数之和相等,![]() ,所以A元素原子的核电荷数为
,所以A元素原子的核电荷数为![]() ,A为硫元素;D元素原子的第一、第二层电子数之和等于其电子总数的一半,所以D元素原子的核电荷数是
,A为硫元素;D元素原子的第一、第二层电子数之和等于其电子总数的一半,所以D元素原子的核电荷数是![]() ,D为钙元素;根据A、B、C、D元素原子的核电荷数依次增大,并都能形成离子,可得B为氯元素,C为钾元素。
,D为钙元素;根据A、B、C、D元素原子的核电荷数依次增大,并都能形成离子,可得B为氯元素,C为钾元素。
(1)A为:S,B为:Cl,C为:K,D为:Ca;它们的原子半径由大到小的顺序是:K>Ca>S>Cl,故答案为:S;Cl ;K;Ca ;K>Ca>S>Cl;
(2)A:![]() ,B:
,B:![]() ,C:
,C:![]() ,D:
,D:![]() ,它们的离子半径由大到小的顺序是S2->Cl->K+>Ca2+,故答案为:
,它们的离子半径由大到小的顺序是S2->Cl->K+>Ca2+,故答案为:![]() ;
;![]() ;
;![]() ;
;![]() ;S2->Cl->K+>Ca2+;
;S2->Cl->K+>Ca2+;
(3)四种元素的最高价氧化物对应水化物的化学式:H2SO4、HClO4、KOH、Ca(OH)2;故答案为:H2SO4、HClO4、KOH、Ca(OH)2;
(4)A为:S,B为:Cl ,其气态氢化物的化学式:H2S、HCl;故答案为:H2S、HCl。


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】废塑料的回收再生利用将工业垃圾变成极有价值的工业生产原料。具有不可忽略的潜在意义。利用如图所示的装置隔绝空气加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,以此探究废塑料的再利用。下列叙述正确的是

A. 聚丙烯的链节是-CH2-CH2-CH2-
B. 装置乙的试管中收集到的物质不能使酸性高锰酸钾溶液褪色
C. 装置丙中的试剂可吸收烯烃且出现溶液分层现象
D. 最后收集的气体可作燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.中和热测定实验中需要的玻璃仪器有:烧杯、量筒、温度计、环形玻璃搅拌棒
B.乙烯的燃烧热为1411.3 kJ·mol1,则乙烯燃烧的热化学方程式为C2H4(g)+3O2(g)![]() 2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
2CO2(g)+2H2O(g) ΔH= 1411.3 kJ·mol1
C.用石墨电极电解1 L 0.1 mol·L1 CuSO4溶液,若反应产生0.1 mol O2,则向原溶液中加入0.2 mol CuO能恢复至原浓度
D.用pH试纸分别测定氯水和盐酸的pH,比较两溶液的酸性强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图,我国学者发现T°C时,甲醇(CH3OH)在铜基催化剂上的反应机理如下:
反应I: CH3OH(g)=CO(g)+2H2 (g) H1=akJ/mol
反应Ⅱ: CO(g)+H2O(g)=CO2 (g)+H2 (g) H2=-bkJ/mol (b>0)
总反应: CH3OH(g)+H2O(g)=CO2 (g)+3H2(g)H3= ckJ/mol

下列有关说法中正确的是( )
A.反应I是放热反应
B.1mol CH3OH(g)和H2O(g)的总能量大于1mol CO2(g)和3mol H2(g)的总能量
C.c>0
D.优良的催化剂降低了反应的活化能,并减少H3,节约了能源。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z均为主族元素,分析表中数据,判断下列说法正确的是(a≠b)( )
元素 | X | Y | Z |
最外层电子数 | a | b | a |
原子半径/nm | 0.154 | 0.130 | 0.211 |
A.X与Y位于同一主族,且X在Y的上一周期
B.X与Z位于同一主族,且X在Z的下一周期
C.X与Z位于同一周期,且X的原子序数小于Z的原子序数
D.X与Z位于同一主族,且X的原子序数小于Z的原子序数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),H=-akJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是( )
4NO(g)+6H2O(g),H=-akJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是( )
A.2分钟反应放出的热量值小于0.1akJ
B.用氧气表示0~2min的反应速率:v(O2)=0.05mol·L-1·min-1
C.2分钟内NH3的转化率是50%
D.2分钟末c(H2O)=0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙可用于治理赤潮、应急供氧等。已知:过氧化钙,为白色或淡黄色结晶粉末,难溶于水,不溶于乙醇、乙醚等有机溶剂,常温下干燥品很稳定,能溶于稀酸生成过氧化氢。某小组同学探究过氧化钙的制法和性质:
(1) 甲、乙两位同学设计的过氧化钙实验室制法如下,其中产率较低的是______(填A、B)
方法A Ca (OH)2 (s) + H2O2 ![]() CaO2 (s) + 2H2O
CaO2 (s) + 2H2O
方法B CaCl2 (s) + H2O2 ![]() CaO2 (s) + 2HCl
CaO2 (s) + 2HCl
方法A所得产品中纯度不高,所含杂质主要是 ___________(填化学式)
如果不加入稳定剂,则两种方法都需在5℃以下进行实验,原因可能是______________。
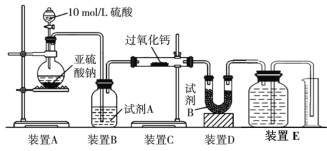
(2) 丙同学认为CO2、SO2与过氧化钙的反应原理相同,丁同学认为SO2具有较强的还原性,而CO2没有,故而反应原理不相同。他们设计了如下实验装置,通过测量装置E中所得气体体积判断反应情况:
①试剂B的作用是____________________。
②若实验中SO2足量,且与过氧化钙充分反应,取反应后的固体进行探究,以验证过氧化钙与SO2反应的生成物。若SO2未被氧化,则反应的化学方程式为:______________________________。
③装置E中收集到的氧气体积为V L(已换算成标准状况下),若SO2完全被氧化,则V =______。
(3)某工厂利用电石渣(主要成分为氢氧化钙)生产过氧化钙的生产流程如下:

①用上述方法制备过氧化钙(CaO2·8H2O),搅拌步骤的化学方程式是______________。
温度(℃) | 50 | 40 | 30 | 20 | 10 | 0 |
产率 | 43.24 | 52.80 | 64.54 | 63.80 | 60.45 | 52.40 |
②某小组釆用单变量法确定温度、H2O2浓度对产率的影响,结果如下:
H2O2 % | 30% | 25% | 20% | 15% | 10% | 5% |
产率 | 60.40 | 62.42 | 64.54 | 63.20 | 63.10 | 62.40 |
则实际生产应选择的适宜条为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案,不能达到相应实验目的的是( )
A | B | C | D | |
实验方案 |
|
|
将NO2球浸泡在冷水和热水中 |
|
实验目的 | 探究反应物浓度对化学平衡的影响 | 探究催化剂对反应速率的影响 | 探究温度对化学平衡的影响 | 比较乙醇中羟基氢原子和水分子中氢原子的活泼性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积为2 L的密闭容器中,加入0.8 mol的A2气体和0.6 mol B2气体,一定条件下发生如下反应:A2(g)+B2(g)![]() 2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是
2AB(g) ΔH<0,反应中各物质的浓度随时间的变化情况如图所示,下列说法不正确的是

A. 图中a点的值为0.15 B. 该反应的平衡常数K=0.03
C. 温度升高,平衡常数K值减小 D. 平衡时A2的转化率为62.5%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com