
| A.砹(At)为有色固体,HAt不稳定 |
| B.铊(T1)是铝的同族元素,原子核外有6个电子层,推测T1(OH)3是两性氢氧化物 |
| C.已知锶Sr与镁同族且原子半径大于钙,硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)比硫化氢稳定性差 |
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源:不详 题型:单选题
| A.NaOH、KOH、CsOH碱性依次增强 |
| B.Li、Na、K、Rb、Cs的失电子能力逐渐增强 |
| C.Al3+、Mg2+、Na+的离子半径依次减小 |
| D.F2、Cl2、Br2、I2的熔沸点依次升高、密度依次增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验方案 (只填写选用试剂序号) | 实验现象 | 结论 | |
| ⑴ | | 一支试管中有白色沉淀生成,另一支试管中先生成白色沉淀,后白色沉淀消失 | 金属性: |
| ⑵ | | | 非金属性:Cl>Br |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
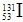 ),初步确认系来自日本核电站事故放射性物质的释放,但这些极微量的放射性物质对我国环境和公众健康不会产生影响,随后东部沿海地区也有类似发现。下列有关说法正确的是
),初步确认系来自日本核电站事故放射性物质的释放,但这些极微量的放射性物质对我国环境和公众健康不会产生影响,随后东部沿海地区也有类似发现。下列有关说法正确的是| A.碘-131是元素碘的一种同位素,正常情况下自然界是不会存在 |
| B.碘-131的化学性质与元素碘不同 |
| C.碘-131的原子核内有74个中子 |
| D.碘元素的相对原子质量是按照包括碘-131在内各种核素原子所占的一定百分比算出的平均值 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.从左到右,原子半径逐渐减小 |
| B.从左到右,元素单质的氧化性减弱,还原性增强 |
| C.从左到右,元素最高正将数从+1递增到+7,负价由—4递变到—1(O、F除外) |
| D.从左到右,元素最高价氧化物对应水化物碱性减弱,酸性增强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性:HI < HBr < HCl < HF | B.稳定性:HF< HCl < HBr < HI |
| C.氧化性:F2 < Cl2 < Br2 < I2 | D.沸点:F2 < Cl2 < Br2 < I2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.若X、Y原子序数相差1,Y为ⅡA族,则X一定是ⅢA族 |
| B.若H n XO m为强酸,则X的氢化物溶液于水一定显酸性 |
| C.若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| D.若Y(OH)m易溶于水,则X(OH)n一定不溶于水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com