
【题目】(1)乙烯使溴水褪色的反应类型和使酸性高锰酸钾溶液褪色的反应类型____(填“相同”或“不相同”)。
(2)用苯制备溴苯的化学方程式是____,该反应的类型___。
(3)已知2CH3CHO+O2![]() 2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
2CH3COOH。若以乙烯为主要原料合成乙酸,其合成路线如图所示。
![]()
则反应②的化学方程式为___,该反应的类型为___。
【答案】不相同 ![]() +Br2
+Br2![]()
![]() +HBr 取代反应 2CH3CH2OH+O2
+HBr 取代反应 2CH3CH2OH+O2![]() 2CH3CHO+2H2O 氧化反应
2CH3CHO+2H2O 氧化反应
【解析】
(1)乙烯与溴水发生加成反应使溴水褪色,酸性高锰酸钾溶液氧化乙烯使高锰酸钾溶液褪色,原理不同、反应类型不同;答案为:不相同。
(2)苯与液溴在Fe作催化剂下反应,苯环上的氢原子被溴原子代替生成溴苯和溴化氢,化学方程式为: 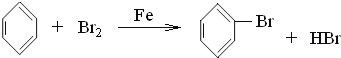 ,属于取代反应;答案为
,属于取代反应;答案为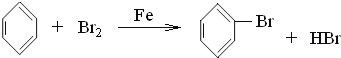 ,取代反应。
,取代反应。
(3)乙烯可以和水加成生成乙醇,所以A是乙醇,乙醇可以被氧化为B乙醛,乙醛易被氧化为C乙酸,乙醇催化氧化为乙醛的方程式为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O,该反应类型是氧化反应;答案为2CH3CH2OH+O2
2CH3CHO+2H2O,该反应类型是氧化反应;答案为2CH3CH2OH+O2![]() 2CH3CHO+2H2O,氧化反应。
2CH3CHO+2H2O,氧化反应。


科目:高中化学 来源: 题型:
【题目】原子结构与性质
(1)元素As与N同族。As的氢化物沸点比NH3的___(填“高”或“低”),其判断理由是______。
(2)铜原子在基态时的价电子排布式为______。
(3)Fe是人体需要补充的元素之一,试写出Fe2+的核外电子排布式:_____。与Al同一周期的Na、Mg元素也是人体所需元素,Na、Mg、Al基态原子第一电离能的大小关系____。某同学所画基态镁原子的核外电子排布图如图![]() ,该同学所画的电子排布图违背了______。
,该同学所画的电子排布图违背了______。
(4)K元素处于元素周期表的____区,其基态原子中,核外电子占据的电子云轮廓图为球形的能级有____个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机A是衡量一个国家石油化学工业的发展水平,D的分子式为C2H5Cl,C是一种常见的高分化合物。请回答下列问题:
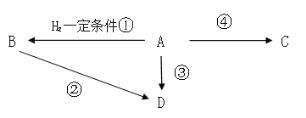
(1)写出A的结构式___;
(2)写出②的方程式___;途径②、③都可以得到D,更合理的是途径___,理由是___;
(3)写出区别A、B两种物质的一种试剂___;
(4)写出④的方程式___;
(5)体育比赛中,当运动员扭伤或肌肉挫伤时,队医随即对准运动员的受伤处喷射液体D(沸点12.27℃)进入局部冷冻麻醉处理,原理是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-—选修3:物质结构与性质]东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是_____。
③氨的沸点(填“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究电化学腐蚀及防护的装置如右图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2 + 2H2O + 4e == 4OH–
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H+ + 2e == H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门实验为基础的科学。请回答下列问题:
(1)利用如图装置可验证浓、稀硝酸氧化性强弱,请完成 实验操作,回答相关问题:
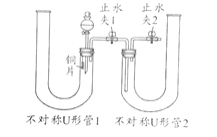
①实验操作过程:固定铜片,打开分液漏斗活塞及止水夹2,从不对称U形管1、2长管口处分别注入稀硝酸、浓硝酸,液面与双孔橡皮塞接触,然后,关闭分液漏斗玻璃活塞、止水夹1、2。此后可观察到现象______;然后打开止水夹1,会发现不对称U形管2中长导管口无色气泡变红棕色,浓硝酸逐渐变黄(说明稀硝酸不能氧化这种无色气体而浓硝酸可以)。
②请用一个化学方程式体现该实验验证浓、稀硝酸氧化性强弱的原理_________。
(2)利用如图装置可以验证非金属性的变化规律。
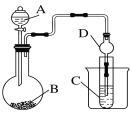
①干燥管D的作用是__________。
②实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置A、B中所装药品分别为________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为______________________。
③若要证明非金属性:Cl > C >Si,则A中加入试剂____________、B中加Na2CO3、C中加入试剂______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
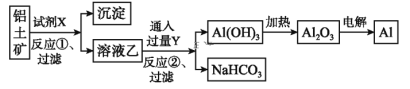
下列叙述正确的是( )
A. 试剂X可以是氢氧化钠溶液,也可以是盐酸
B. 反应①过滤后所得沉淀为氢氧化铁
C. 图中所示转化反应都不是氧化还原反应
D. 反应②的化学方程式为NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测定H2C2O4·xH2O 中x值: 已知:M(H2C2O4)=90 g·mol-1
①称取 1.260 g H2C2O4·xH2O晶体,将其配成100.00 mL 水溶液为待测液;
②量取 25.00mL 待测液放入锥形瓶中,再加入适量的稀H2SO4;
③用20.00ml浓度为 0.05000 mol·L-1的 KMnO4标准溶液进行滴定。
(提示:H2C2O4被氧化为CO2 , KMnO4被还原为MnSO4)
(1)请写出与滴定有关反应的化学方程式______________。
(2)某学生的滴定方式(夹持部分略去)如下,最合理的是_____(选填 a、b)。
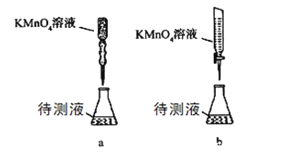
(3)滴定过程中眼睛应注视______________________。
(4)通过上述数据,求得x=____________。以标准KMnO4溶液滴定样品溶液的浓度,未用标准KMnO4溶液润洗滴定管,引起实验结果______(偏大、偏小或没有影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组选用酸性高锰酸钾溶液和草酸(H2C2O4)溶液,探究外界条件对化学反应速率的影响,进行了如下三组实验:[实验内容及记录]
已知:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
_mol·L-1H2C2O4溶液 | H2O | 0.05 mol·L-1KMnO4溶液 | 3 mol·L-1稀硫酸 | ||
1 | 3.0 | 1.0 | 4.0 | 2.0 | 4.0 |
2 | 2.0 | 2.0 | 4.0 | 2.0 | 5.2 |
3 | 1.0 | 3.0 | 4.0 | 2.0 | 6.4 |
请回答:
(1)[实验原理]_____________(写离子方程式)。
(2)为完成实验目的,H2C2O4溶液的物质的量浓度不低于________。
(3)根据上表中的实验数据,可以得到的结论是_________。
(4)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示,但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设。并继续进行实验探究。

①该小组同学提出的假设是__________。
②请你帮助该小组同学完成实验方案。
实验 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量MnSO4 | 室温下溶液颜色褪至无色所需时间/min | |||
__mol·L-1 H2C2O4溶液 | H2O | 0.05 mol·L-1 KMnO4溶液 | 3 mol·L-1 稀硫酸 | |||
4 | 3.0 | 1.0 | 4.0 | 2.0 | 0.1 g | t |
若该小组同学提出的假设成立,应观察到的现象_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com