
【题目】下列反应属于氧化还原反应,且在反应中水只作为还原剂的是( )
A.3Fe+4H2O(g)![]() Fe3O4+4H2B.2H2O
Fe3O4+4H2B.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C.Na2O+H2O═2NaOHD.2F2+2H2O═4HF+O2
【答案】D
【解析】
A. 反应中,H2O中H元素化合价从+1价降低到0价,得到电子;
B. 反应中,H2O中H元素化合价从+1价降低到0价,O元素化合价从-2价升高到0价;
C. 反应中没有化合价变化;
D. 反应中,H2O中O元素化合价从-2价升高到0价;
A. 反应3Fe+4H2O(g)![]() Fe3O4+4H2中,H2O中H元素化合价从+1价降低到0价,得到电子,H2O作氧化剂,A项错误;
Fe3O4+4H2中,H2O中H元素化合价从+1价降低到0价,得到电子,H2O作氧化剂,A项错误;
B. 反应2H2O![]() 2H2↑+O2↑中,H2O中H元素化合价从+1价降低到0价,O元素化合价从-2价升高到0价,H2O既做氧化剂又作还原剂,B项错误;
2H2↑+O2↑中,H2O中H元素化合价从+1价降低到0价,O元素化合价从-2价升高到0价,H2O既做氧化剂又作还原剂,B项错误;
C. 反应Na2O+H2O═2NaOH中没有化合价变化,不属于氧化还原反应,C项错误;
D. 反应2F2+2H2O═4HF+O2中,H2O中O元素化合价从-2价升高到0价,H2O作还原剂,D项正确;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达不正确的是
A. 在基态多电子原子中,p轨道电子能量不一定高于s轨道电子能量
B. 核外电子排布由1s22s22p63s1→1s22s22p6 的变化需要吸收能量
C. 某元素基态原子的电子排布图![]()
D. Ca2+离子基态电子排布式为1s22s22p63s23p6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积恒定的密闭容器中发生可逆反应A(g)+3B(g) ![]() 2C(g),下列叙述一定是达到平衡的标志的是
2C(g),下列叙述一定是达到平衡的标志的是
①2υ(B)正=3υ(C)逆;②单位时间内生成a mol A,同时消耗2a mol C;③A、B、C的浓度不再变化;④混合气体的总压强不再变化;⑤C的质量分数不再改变;⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2的状态;⑦A、B、C的浓度彼此相等;⑧混合气体的密度不再改变的状态
A. ①③④⑤ B. ①④⑤⑦ C. ④⑤⑥⑧ D. ③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】180℃时将0.5 mol H2和1 mol CO2通入1 L的恒容密闭容器中,反应生成甲醇蒸汽(CH3OH)和某无机副产物,测得各物质的物质的量随时间的部分变化如图所示,下列说法中正确的是

A. 该反应的化学方程式:2CO2+4H2![]() 2CH3OH+O2
2CH3OH+O2
B. 在0~3 min内H2的平均化学反应速率为0.1 mol·L-1·min-1
C. 当容器内混合气体密度不再变化时,表明反应已经达到平衡状态
D. 在3~10 min内,反应仍未达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定Na2CO3和NaHCO3混合物样品的组成,称取不同质量样品溶于水后分别逐滴加入相同浓度盐酸30 mL,充分反应,产生CO2的体积(已折算成标准状况下的体积)与加入样品的质量关系如图所示(不考虑CO2在水中的溶解、反应)。请计算:

(1)样品中n(Na2CO3) : n(NaHCO3)=____________。
(2)盐酸的物质的量浓度c(HCl)=________mol·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应可视为旧键的断裂和新键的形成过程。化学键的键能是形成化学键时释放的能量。已知白磷和P4O6的分子结构如图所示,现提供以下化学键的键能(kJ·mol-1):P—P:198P—O:360O=O:498,则反应P4(白磷)+3O2=P4O6的反应热ΔH为 ( )

A. -1638 kJ·mol-1B. +1638 kJ·mol-1C. -126 kJ·mol-1D. +126 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。
(1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。
①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。
②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。
③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。
(2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。
a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小
(3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。

图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。
图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某待测液中可能含有大量Mg2+、Cu2+、Fe3+、K+、H+、NO3-、SO42-、OH-离子中的一种或几种,现通过下实验进行检验:
①取少量待测液,仔细观察,呈无色;
②向上述待测液中滴加NaOH溶液,先无明显现象,后有白色沉淀生成,
③向上述溶液中加入BaCl2溶液,无现象。
据此可以判断该待测液中一定大量存在的离子是_______,一定不能大量存在的离子是_______,不能确定是否存在的离子是___________。
(2)标准状况下,H2和CO的混合气体共8.96L,测得其质量为6.0g,试计算此混合气体中H2的质量为___________,CO体积为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业综合处理含![]() 废水和含
废水和含![]() 的废气,得无毒气体b,流程如下:
的废气,得无毒气体b,流程如下:
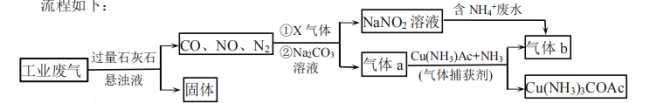
下列说法错误的是( )
A.“固体”中主要含有![]() 、
、![]()
B.X气体、![]() 与
与![]() 溶液的离子反应:
溶液的离子反应:![]()
C.处理含![]() 废水时,离子反应:
废水时,离子反应:![]()
D.捕获剂捕获气体a中![]() 发生了氧化还原反应
发生了氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com