
| A、BaSO4 |
| B、BaCO3 |
| C、BaCl2 |
| D、NaCl |
科目:高中化学 来源: 题型:
| A、降低温度 |
| B、增大H2的浓度 |
| C、增大压强 |
| D、减小压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钙溶于醋酸溶液中:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氯化镁溶液和氨水混合:Mg2++2OH-=Mg(OH)2 |
| C、铁与稀硫酸反应:2Fe+6H+═2Fe3++H2↑ |
| D、铜片插入硝酸银溶液中 Cu+2Ag+=Cu2++2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胶体有电泳现象原因是胶体带电 |
| B、胶体不稳定,静置后容易产生沉淀 |
| C、胶体的本质特征是丁达尔效应 |
| D、胶粒做不停的,无秩序的运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量的浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+=Cu2++2Fe2+ |
| C、大理石溶于醋酸中的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
| D、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、低碳经济是尽可能地减少煤炭石油等高碳能源消耗,减少温室气体排放 |
| B、发展太阳能经济有助于减缓温室效应 |
| C、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| D、植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下.5.6克Fe投入到浓硝酸中,生成0.1NA的Fe3+ |
| B、0.1 mol的白磷(P4)或甲烷分子中所含的共价键数均为0.4NA |
| C、在精炼铜或电镀铜的过程中,当阴极都析出32 g铜时转移电子数均为NA |
| D、通过MnO2催化使H2O2分解,产生32g O2时转移电子数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
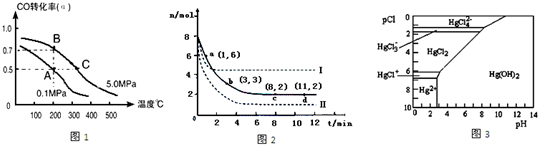
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com