
【题目】有三份不同质量的铁粉样品①②③,甲、乙、丙三位同学各取一份样品分别与含有0.8molHNO3的稀硝酸反应,反应后硝酸和铁均无剩余,且硝酸的还原产物只有NO。据此回答下列问题:
(1)甲取样品①,反应后的溶液中铁只以 Fe3+离子的形式存在,则样品①的质量为_________g。
(2)乙取样品②,反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量 (设为ag)范围是________。
(3)丙取样品③,将其慢慢加入到稀硝酸中,并不断搅拌,反应过程中溶液里Fe3+、Fe2+、NO3三种离子中的一种离子的物质的量的变化曲线如下图所示,则该曲线表示的是物质的量变化的曲线,请你在此图中再画出另外两种离子的物质的量的变化曲线。
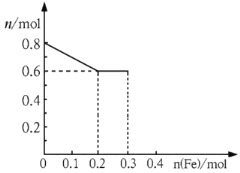
【答案】
(1)11.2
(2)11.2<a<16.8 或 11.2g<ag<16.8g
(3)NO3(1分)如下图
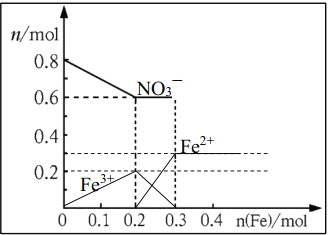
【解析】
试题分析:(1)设Fe的物质的量是x,则生成硝酸铁也是x,所以被还原的硝酸是0.8mol-3x,根据电子的得失守恒可知,3x=3×(0.8mol-3x),解得x=0.2mol,所以铁的质量是0.2mol×56g/mol=11.2g。
(2)如果铁的氧化产物是亚铁离子,则生成硝酸亚铁是2x,所以被还原的硝酸是0.8mol-2x,
根据电子的得失守恒可知,2x=3×(0.8mol-2x),解得x=0.3mol,所以铁的质量是0.3mol×56g/mol=16.8g,因此如果是反应后的溶液中既含有Fe3+、又含有Fe2+离子,则样品②的质量是11.2<a<16.8;
(3)由于最初溶液中NO3-的物质的量就是0.8mol,所以曲线表示的是NO3-的物质的量变化的曲线;根据反应的方程式Fe+4HNO3=Fe(NO3)3+NO↑+2H2O、2Fe(NO3)3+Fe=3Fe(NO3)2可知,铁离子的最大值是0.2mol。如果继续加入铁,则开始生成亚铁离子,亚铁离子的最大值是0.3mol。


科目:高中化学 来源: 题型:
【题目】将Y1L的H2和Y2L的N2在一定条件下发生反应,达到平衡后,混合气体总体积为Y3L(气体体积均在相同条件下测定),则生成NH3的体积是
A.(Y1+Y2-Y3)L B.(Y1+Y2+Y3)L C.(Y1+ Y2-2Y3)L D.[Y3-(Y1+Y2)]L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和盐酸,各加入生铁块,放置一段时间。下列有关描述错误的是
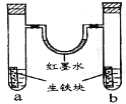
A.生铁块中的碳是原电池的正极
B.红墨水柱两边的液面变为左低右高
C.两试管中负极电极反应相同
D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分类法是交叉分类法的是( )
A.氧化物可分为金属氧化物和非金属氧化物
B.S2-、I-、NH4+、SO42-按某种属性可分为两类
C.氢氧化钙既是纯净物又是化合物,属于碱
D.物质的分离方法可分为蒸馏、分液、蒸发、萃取、过滤等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将乳清蛋白、淀粉、胃蛋白酶、唾液淀粉酶和适量水混合装入一容器内,调整pH值2.0,保存于37℃的水浴锅内。过一段时间后,容器内剩余的物质是
A. 淀粉、胃蛋白酶、多肽、水
B. 唾液淀粉酶、胃蛋白酶、多肽、水
C. 唾液淀粉酶、麦芽糖、胃蛋白酶、多肽、水
D. 唾液淀粉酶、淀粉、胃蛋白酶、水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 蛋白质、蔗糖、油脂在一定条件下都能水解
B. 乙酸、乙醇都能与钠反应产生H2
C. 乙烯和聚丙烯都能使酸性高锰酸钾溶液褪色
D. 分子式为C6H6的有机物可能是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷和红磷均能在空气中燃烧,且燃烧产物相同,但二者的燃烧热不同,通过实验可测得这两个反应的反应热。
①![]() P4(s,白磷)+
P4(s,白磷)+![]() O2(g)===
O2(g)===![]() P4O10(s) ΔH1=-745.8 kJ·mol-1
P4O10(s) ΔH1=-745.8 kJ·mol-1
②4P(s,红橉)+5O2(g)===P4O10(s) ΔH2=-2954 kJ·mol-1
(1)白磷和红磷的关系是_____________。
a.同一种物质 b.同位素 c.同分异构体 D.同素异形体
(2)红磷的燃烧热是________kJ·mol-1,白磷的燃烧热比红磷的燃烧热___________(填“大”或“小”)。
(3)白磷转化为红磷的热化学方程式为P4(s,白磷)===4P(s,红磷)ΔH=-29.2 kJ·mol-1。在相同的条件下,能量较低的是________(填“白磷”或“红磷”),白磷的稳定性比红磷________(填“高”或“低”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com