
用双线桥表示下列反应中得失电子的情况,并按要求回答:
3FeO + 10HNO3 = 3Fe(NO3)3 + NO↑ + 5H2O.
(1)氧化剂是 ;氧化产物是 。
(2)在参加反应的硝酸中,起氧化剂(被还原)作用的HNO3与起酸性作用的HNO3的质量比为 。
(3)用双线桥标明电子转移的方向和数目 。
(1)HNO3,Fe(NO3)3 (2)1:9
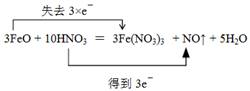
(3)
【解析】
试题分析:(1)得到电子,所含元素化合价降低的反应物是氧化剂,氧化剂被还原生成还原产物。反之就是失去电子,所含元素化合价升高的反应物是还原剂,还原剂被氧化生成氧化产物。根据方程式可知,铁元素的化合价从+2价升高到+3价,所以氧化亚铁是还原剂,硝酸铁是氧化产物;硝酸中氮元素的化合价从+5价降低到+2价,得到电子,因此硝酸是氧化剂,NO是还原产物。
(2)如果设氧化亚铁是1mol,则生成1mol硝酸铁,即没有被还原的硝酸是3mol。根据电子的得失守恒可知,被还原的硝酸是1mol÷3,所以在参加反应的硝酸中,起氧化剂(被还原)作用的HNO3与起酸性作用的HNO3的质量比1/3︰3=1︰9。
(3)用双线桥标明电子转移的方向和数目起点和终点都是同一种元素,所以根据(1)、(2)分析可知,应该是
考点:考查氧化还原反应的有关判断、计算及表示等
点评:在进行氧化还原反应的有关判断计算时,应该仅仅抓住电子得失守恒这一关系式进行列式计算。


 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源:2011-2012学年广东省培正中学高一上学期期中考试化学试卷 题型:填空题
(12分)用双线桥表示下列反应中得失电子的情况,并指明氧化剂、还原剂、氧化产物、还原产物:
3FeO + 10HNO3 ="== " 3Fe(NO3)3 + NO↑ + 5H2O
( ) ( ) ( ) ( )
其中,氧化性:__________ > ___________ ;还原性:___________ > ___________
查看答案和解析>>
科目:高中化学 来源:2012-2013学年陕西宝鸡金台高一上学期期中质量检测化学试卷(带解析) 题型:填空题
用双线桥表示下列反应中得失电子的情况,并按要求回答:
3FeO + 10HNO3= 3Fe(NO3)3 + NO↑ + 5H2O.
(1)氧化剂是 ;氧化产物是 。
(2)在参加反应的硝酸中,起氧化剂(被还原)作用的HNO3与起酸性作用的HNO3的质量比为 。
(3)用双线桥标明电子转移的方向和数目 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com