
【题目】(1)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)![]() (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)![]() NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3 与 ΔH1、ΔH2 之间的关系是:ΔH3=________。
(2)白磷与氧气反应生成P4O10 固体 。下表所示是部分化学键的键能参数:
化学键 | P—P | P—O | P===O | O===O |
键能/kJ·mol-1 | a | b | c | d |
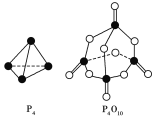
根据右图的分子结构和有关数据通过计算写出该反应的热化学方程式为 。
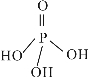
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右下图)之间脱去两个水分子产物,其结构式为_________________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为____________。
(4)已知298 K时白磷不完全燃烧的热化学方程式为:
P4(s,白磷)+3O2(g)===P4O6(s) ΔH=-1 638 kJ·mol-1。
在某密闭容器中加入62 g白磷和50.4 L氧气(标准状况),控制条件使之恰好完全反应。则所得到的P4O10与P4O6的物质的量之比为________。
【答案】(1)2ΔH2-ΔH1
(2) P4(s)+5O2(g)===P4O10(s) △H= - ( 4c + 12b - 6a - 5d ) kJ·mol-1
(3)![]() ,Na5P3O10(4)3∶1
,Na5P3O10(4)3∶1
【解析】
试题分析:(1)将反应Ⅰ倒过来书写:(NH4)2CO3 (aq)2NH3 (l)+H2O (l)+CO2 (g)-△H1
将反应Ⅱ×2:2NH3 (l)+2H2O (l)+2CO2 (g)2NH4HCO3 (aq) 2△H2
得:(NH4)2CO3 (aq)+H2O (l)+CO2 (g)2NH4HCO3 (aq)△H3=2△H2-△H1 ;
(2)依据键能的数值可以估算化学反应的热效应,即△H=反应物的键能总和-生成物的键能总和。根据反应P4+5O2═P4O10,并结合物质的结构式可知,白磷分子中含有6个P-P键,氧气中含有1个O=O键,P4O10分子中含有4个P=O键和12个P-O键,因此该反应的△H=6a+5d-(4c+12b),因此P4(s)+5O2(g)===P4O10(s) △H= - ( 4c + 12b - 6a - 5d ) kJ·mol-1。
(3)三聚磷酸可视为三个磷酸分子之间脱去两个水分子产物,其结构式为![]() ,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10;
,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10;
(4)设得到的 P4O10 与 P4O6 的物质的量分别为 x mol、y mol。则 x+y=0.5,5x+3y=2.25,解得 x=0.375,y=0.125。物质的量之比为3:1。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. C与Si位于同一主族,且干冰与SiO2都是酸性氧化物 ,所以二者晶体类型相同
B. NaCl和AlCl3均为强电解质,二者在熔融状态下都能导电
C. 从晶体类型上来看物质的熔沸点,其规律是:原子晶体>离子晶体>分子晶体
D. 第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验,所得实验现象和实验结论正确的是( )
实验 | 现象 | 实验结论 | |
A | 将SO2气体通入紫色石蕊试液中 | 溶液先变红后褪色 | 二氧化硫具有酸性和漂白性 |
B | 将小苏打和硫酸应生成的气体,通入一定浓度的Na2SiO3溶液中 | 出现白色胶状沉淀 | 酸性: H2SO4﹥H2CO3﹥H2SiO3 |
C | 将光亮的镁条放入盛有NH4Cl溶液的试管中 | 有大量气泡产生 | 反应中有NH3产生 |
D |
| 试管a出现白色沉淀, 试管b出现黄色沉淀 | 溶度积:Ksp(AgCl)﹥Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
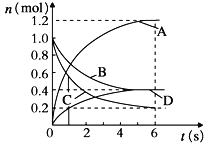
A.该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 常温常压下,8g O2含有4NA个电子
B. 1L 0.1mol·L-1的氨水中有0.1NA个NH4+
C. 标准状况下,22.4L四氯化碳含有NA个分子
D. 1molNa被完全氧化生成Na2O2,失去2NA电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于海水资源综合利用的说法中,不正确的是( )
A.从海水中富集镁元素可用Ca(OH)2沉淀法
B.海水淡化的方法主要有蒸馏法、离子交换法、电渗析法
C.从海水中提取溴单质的过程中用氯气做还原剂
D.从海水中获得粗盐可用蒸发结晶法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蛋白质的性质在生活中有许多实际应用.请在下表“性质”一栏中表述的蛋白质性质填空.
实例 | 性质 |
(1)紫外线消毒 | 变性 |
(2)蛋白质遇浓硝酸变黄 | |
(3)误食了重金属离子,可以立即喝大量的牛奶来缓解毒性 | |
(4)鸡蛋清溶液中加入少量饱和的硫酸铵溶液出现沉淀 | |
(5))常用酒精清洗伤口 | |
(6)蒸煮鸡蛋食用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“绿色化学”的核心是在化学反应过程中或化工生产中,尽量减少使用或彻底消除有害物质,下列做法中,符合“绿色化学”理念的是 ( )
A.生产和使用剧毒农药 B.化工厂产生的废气向高空排放
C.利用氢气作高能燃料 D.造纸厂用二氧化硫进行纸浆漂白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,已知Cu3P中P为-3价,则15molCuSO4可氧化的P的物质的量为
A. 1.5mol B. 5.5mol C. 3mol D. 2.5mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com