
| A. | 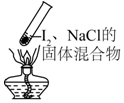 加热时,上部汇聚了固体碘,说明碘的热稳定性较差 | |
| B. | 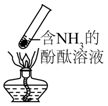 加热时,中部溶液变红,冷却后又变为无色 | |
| C. | 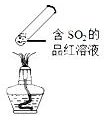 加热时,中部溶液变红,冷却后又变为无色 | |
| D. |  \加热时,上部汇聚了白色固体,说明氯化铵易升华 |
分析 A.碘单质易升华,属于碘单质的物理性质,不能据此判断碘的热稳定性;
B.加热时氨气逸出,溶液颜色为无色,冷却后氨气溶解溶液为红色;
C.二氧化硫具有漂白性,加热后溶液变红,冷却后溶液褪色;
D.氯化铵不稳定,加热分解生成氨气和氯化氢.
解答 解:A.加热时,①上部汇集了固体碘单质,说明碘发生了升华现象,为其物理性质,不能说明碘单质的热稳定性较差,故A错误;
B.氨水呈碱性,加热后溶液呈无色,冷却后溶液呈红色,故B错误;
C.加热后二氧化硫逸出,溶液呈红色,冷却后二氧化硫又将品红溶液漂白,故C正确;
D.加热时,氯化铵分解生成HCl和氯气,氨气与氯化氢冷却后又生成氯化铵,则上部汇聚了白色固体,说明氯化铵不稳定,而不是升华,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及升华、稳定性、漂白性等知识,明确常见化合物性质为解答关键,试题培养了学生的分析能力及化学实验能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 分别同时滴入等浓度的盐酸,放出气体NaHCO3比Na2CO3快 | |
| B. | 热稳定性Na2CO3<NaHCO3 | |
| C. | 常温时水溶性Na2CO3<NaHCO3 | |
| D. | 相对分子质量Na2CO3<NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、MnO4-、Cl-、SO42- | B. | Na+、AlO2-、Cl-、SO42- | ||
| C. | SO42-、Fe3+、HCO3-、Ba2+ | D. | Mg2+、NO3-、NH4+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及对离子方程式 | 评价 |
| A | 金属钠加入滴有酚酞的水中:Na+H2O═Na++OH-+H2↑ | 正确 |
| B | 等体积等物质的量浓度的AlCl3、Ba(OH)2、HCl溶液混合:Al3+3H+6OH-═Al(OH)3↓+3H2O | 正确 |
| C | 向硅酸钠溶液中通入过量CO2:SiO32-+2H2O+2CO2═H2SiO3↓+2HC3-O | 错误,CO2过量溶液应该变澄清 |
| D | 向氯化钠铝溶液中加入足量氨水溶液:Al3++4NH3•H2O═AlO2+2H2O+4NH4+ | 正确 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
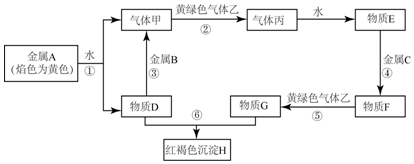
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
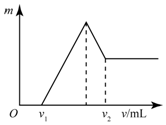 (1)为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将100g样品加热使其质量不再变化,其质量变为96.9%,则该样品的纯度(质量分数)是91.6%
(1)为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将100g样品加热使其质量不再变化,其质量变为96.9%,则该样品的纯度(质量分数)是91.6%查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A的转化率变大 | B. | a<c+d | ||
| C. | A的质量分数变小 | D. | 平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com