
| A、6.8g熔融的KHSO4中含有0.1NA个阳离子 |
| B、0.1mol Na2O2晶体中含有0.1NA个阴离子 |
| C、在25℃时,1L 1mol/L醋酸溶液中所含分子的个数大于NA |
| D、在标准状况下的22.4L辛烷完全燃烧,生成的二氧化碳的分子数为8NA |
| 6.8g |
| 136g/mol |


科目:高中化学 来源: 题型:
| A、在水中加KHCO3 |
| B、在水中加HCl |
| C、在水中加CuCl2 |
| D、将水加热至100℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 100mL稀盐酸 |
| NaOH溶液 |
| 100mLNaOH溶液 |
| 稀盐酸 |
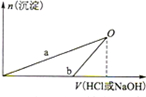 下列说法正确的是( )
下列说法正确的是( )| A、X溶液和Y溶液中均只含一种溶质 |
| B、b曲线表示的是向X溶液中加入NaOH溶液 |
| C、在O点时两方案中所得溶液浓度相等 |
| D、a、b曲线表示的反应都是复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的有机物,下列关于它的说法错误的是( )
的有机物,下列关于它的说法错误的是( )| A、分子式为C10H16 |
| B、属于苯的同系物 |
| C、能使溴水褪色 |
| D、难溶于水,且密度比水大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷和丙烯 |
| B、甲烷和2-丁烯 |
| C、甲烷和乙烯 |
| D、乙烯和1-丁烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蓝色 | B、黄色 | C、红色 | D、橙色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3-C*H2-CH3 |
| B、C*H2=CH-CH3 |
| C、CH2=C*H-CH3 |
| D、CH2=CH-C*H3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com