
����Ŀ��ij�ϴ�����SiO2��ZnS��CuS��������Fe3O4��ijʵ��С���Ը÷ϴ���Ϊԭ�ϣ�����п��ͭ�����ʵ��������ͼ��
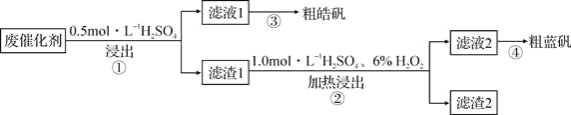
����˵����ȷ���ǣ� ��
A.������Һ1���Ƿ���Fe2+������ѡ��KSCN�����Ƶ���ˮ
B.����ڲ����У�Ӧ�ȼ�6%H2O2��Ȼ�Ͻ����»�������1.0mol/LH2SO4
C.����1�ɷ���SiO2��CuS������2�ɷ�ֻ��SiO2
D.����ٲ����У����ɵ���������NaOH��Һ��CuSO4��Һ����
���𰸡�D
��������
�ϴ�������ϡ���ᣬ��һ�ν�����Ҫ������ӦZnS+H2SO4=ZnSO4+H2S����Fe3O4+4H2SO4=FeSO4+Fe2(SO4)3+4H2O�����˺���Һ��ZnSO4��FeSO4��Fe2(SO4)3��Ũ���ᾧ�õ���ZnSO4��7H2O������1����SiO2��CuS����ʢ������1�ķ�Ӧ���м�H2SO4��H2O2��Һ������������ԭ��Ӧ����������ͭ��������2������Ͷ������裬��Һ��������ͭ����Ũ����ᾧ�ɵõ�����ͭ���壬�Դ˽����⡣
A.��Һ1�п��ܺ���Fe2+��������Fe3+������KSCN�����Ƶ���ˮ���ܼ����Ƿ�Fe2+����A����
B.�������������������¿�����CuS��Ӧ�ȼ���ϡ���ᣬ�ټ���������⣬��B����
C.����2������Ͷ������裬��C����
D.����ٲ��������ɵ�����Ϊ���⣬����NaOH��Һ��CuSO4��Һ���գ���D��ȷ��
�ʴ�ѡD��


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£�ˮ��Һ��H����OH����Ũ�ȱ仯������ͼ������˵����ȷ����(����)
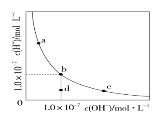
A.�����¶ȣ�����������c��b�ı仯
B.���¶��£�ˮ�����ӻ�����Ϊ1.0��10��13
C.���¶��£�����FeCl3����������b��a�ı仯
D.���¶��£�ϡ����Һ����������c��d�ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() N2(g)+
N2(g)+![]() H2(g)=N(g)+3H(g) ��H1=+akJ��mol-1��
H2(g)=N(g)+3H(g) ��H1=+akJ��mol-1��
N(g)+3H(g)=NH3(g) ��H2=-bkJ��mol-1��
NH3(g)=NH3(l) ��H3=-ckJ��mol-1
��д��N2(g)��H2(g)��Ӧ����Һ�����Ȼ�ѧ����ʽ��__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����������ữ�ĸ��������Һ������������Һ��ϣ���ַ�Ӧ������������Һ�м���KI��Һ�������Һ�������ӵ����ʵ���������KI�����ʵ����ı仯��ϵ��ͼ��ʾ���������й�˵������ȷ����
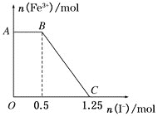
A.ͼ��AB����Ҫ�Ǹ�����غ͵⻯����Һ��Ӧ
B.ͼ��BC�η����ķ�ӦΪ2Fe3����2I��=2Fe2����I2
C.����OC�ε����ݿ�֪��ʼ����ĸ�����ص����ʵ���Ϊ0.25 mol
D.����OC�ε����ݿ�֪��ʼ������������������ʵ���Ϊ1 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H2O2�ķֽ�����Ӱ�����ؽ����о�������ͬ�¶��£�ʵ���ò�ͬ�����³�O2Ũ����ʱ��仯��ͼ��ʾ������˵������ȷ���ǣ� ��
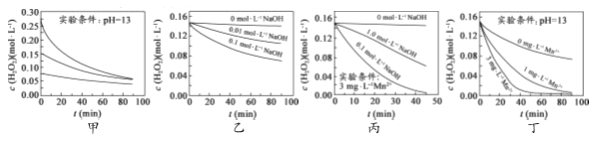
A. ͼ�ױ�������ͨ���ʵ�����H2O2Ũ�ȣ��ӿ�H2O2�ֽ�����
B. ͼ�ұ�������ͨ��������Һ������ԣ�����H2O2�ֽ����ʿ���
C. ͼ��������Mn2+��������ʱ������̫ǿ��������H2O2�ֽ�
D. ͼ�ҡ�ͼ����ͼ��������Mn2+��H2O2�ֽ�Ĵ��������Mn2+��Ũ�Ⱦ�������H2O2 �ֽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��X(g)��3Y(g)![]() 2Z(g)��һ�������£�0.3 mol X(g)��0.3 mol Y(g)�����Ϊ1 L���ܱ������з�����Ӧ������ͼʾ��������
2Z(g)��һ�������£�0.3 mol X(g)��0.3 mol Y(g)�����Ϊ1 L���ܱ������з�����Ӧ������ͼʾ��������
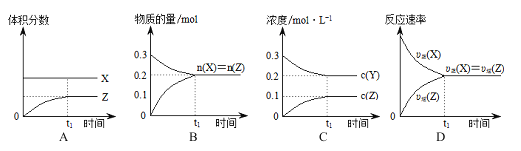
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�����A��B�����2L���ܱ������У��������з�Ӧ��3A(g)+B(g)![]() xC(g)+2D(g)����2min����D��Ũ��Ϊ0.5mol/L��c(A)��c(B)��3��5����C��ʾ��ƽ������v(C)��0.25mol��L1��min1������˵����ȷ����
xC(g)+2D(g)����2min����D��Ũ��Ϊ0.5mol/L��c(A)��c(B)��3��5����C��ʾ��ƽ������v(C)��0.25mol��L1��min1������˵����ȷ����
A. ��Ӧ����v(B)��0.25 mol��L��1��min��1
B. �÷�Ӧ����ʽ��x��1
C. 2minʱ��A�����ʵ���Ϊ1.5mol
D. 2minʱ��A��ת����Ϊ60%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼʾ���Ӧ�������������
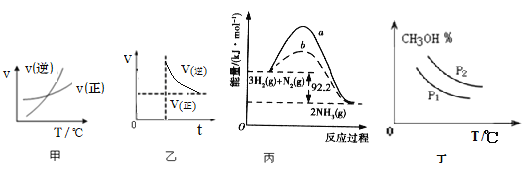
A.��ͼ�ױ�ʾ�ķ�Ӧ�������¶ȱ仯�Ĺ�ϵ��֪�÷�Ӧ����H��0
B.ͼ�ұ�ʾ��ӦNH2COONH4(s) ![]() 2NH3(g)+CO2(g)�ﵽƽ�������ѹǿ����Ӧ���ʺ�ʱ��Ĺ�ϵ���ﵽ��ƽ�����Ũ�Ȳ��䣬ѹǿҲ����
2NH3(g)+CO2(g)�ﵽƽ�������ѹǿ����Ӧ���ʺ�ʱ��Ĺ�ϵ���ﵽ��ƽ�����Ũ�Ȳ��䣬ѹǿҲ����
C.ͼ���������г��� 1 mol N2��3 mol H2����ַ�Ӧ��ų����� 92.2 kJ
D.ͼ���ɱ�ʾ�ڲ�ͬѹǿP1��P2(P1>P2)������CO(g)+2H2(g) ![]() CH3OH(g) ��H��0���״��ٷֺ������¶ȱ仯�����
CH3OH(g) ��H��0���״��ٷֺ������¶ȱ仯�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ2C+O2=2CO�������仯��ͼ��ʾ������˵����ȷ���ǣ� ��
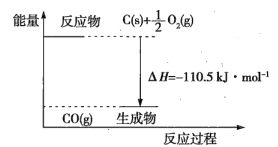
A.12gC(s)��һ����O2(g)��Ӧ����14gCO(g)�ų�������Ϊ110.5kJ
B.2molC(s)������O2(g)��Ӧ����CO2(g)�ų�����������221kJ
C.�÷�Ӧ���Ȼ�ѧ����ʽ��2C(s)+O2(g)=2CO(g) ��H=-221kJ
D.�÷�Ӧ�ķ�Ӧ�ȵ������ɵ�CO(g)�������е�������μӷ�Ӧ��O2(g)�������е������IJ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com