
| A、2,2-二甲基丁烷的一氯代物有3种 |
| B、乙烯与苯都存在碳碳双键 |
| C、可用酸性KMnO4溶液鉴别苯、甲苯、己烯与四氯化碳 |
| D、等物质的量的乙烯与乙醇完全燃烧时,其耗氧量不相同 |


科目:高中化学 来源: 题型:
A、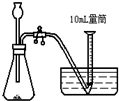 |
B、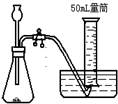 |
C、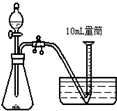 |
D、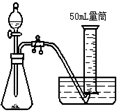 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH2OH和CH3-O-CH3 |
| B、H2NCH2COOH和CH3CH2NO2 |
| C、CH3CH2COOH和CH3COOCH3 |
| D、CH3CH3和CH3CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、足量6mol/L NaOH溶液 |
| B、少量6mol/L H2SO4溶液 |
| C、少量NaHCO3固体 |
| D、足量Na2SO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中溶质是Na2CO3和NaOH |
| B、溶液中的离子浓度:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| C、溶液中的离子浓度:c(Na+)>c(HCO3-)=c(CO32-)>c(OH-)>c(H+) |
| D、溶液中的离子浓度:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热 |
| B、小心加入少量98%浓硫酸 |
| C、滴加少量Na2SO4溶液 |
| D、不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
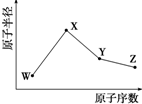 W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示.已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的原子半径在同周期主族元素中最小.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com