
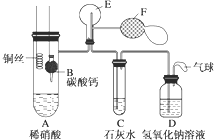
分析 实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色,且在C中可观察到浑浊,有碳酸钙沉淀生成,A中硝酸和铜反应生成NO,易于氧气反应,则将F气球中空气压入E中,有红棕色气体生成,装置D中盛有氢氧化钠溶液,可用与吸收二氧化氮气体,气体中气球可用于吸收不反应的NO,以防止污染空气,以此解答该题.
解答 解:(1)实验时,可先将B装置中CaCO3放入硝酸中,碳酸钙和硝酸反应生成二氧化碳气体,先排出去其中的空气,以便在E烧瓶中收集到NO,以便观察颜色,
故答案为:B装置中CaCO3放入硝酸中;
(2)A中硝酸和铜反应生成NO,易于氧气反应,则将F气球中空气压入E中,有红棕色气体生成,如观察到红棕色,则说明生成NO而不是氢气,
生成二氧化氮通入C中生成硝酸,硝酸与碳酸钙反应,反应的化学方程式为2HNO3+CaCO3═Ca(NO3)2+CO2↑+2H2O,
故答案为:将F气球中空气压入E中,有红棕色气体生成;2HNO3+CaCO3═Ca(NO3)2+CO2↑+2H2O;
(3)装置D中盛有氢氧化钠溶液,可用与吸收二氧化氮气体,气体中气球可用于吸收不反应的NO,以防止污染空气,故答案为:吸收多余的NO、NO2;
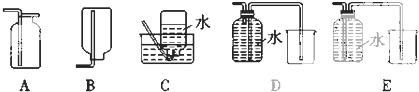
(4)NO易与氧气反应,不能用排水法收集,一般用排水法收集,可用C、D装置,E的进气管太长,不能将水排出,故答案为:CD.
点评 本题以硝酸的性质为载体综合考查性质实验的设计,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握相关物质的性质,明确实验目的和原理是解答该题的关键,注意相关实验操作方法的注意事项,难度中等.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键 | |
| B. | 碳原子性质活泼,可以跟多数元素原子形成共价键 | |
| C. | 碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和叁键 | |
| D. | 多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低 | |
| B. | 实验室中常用排饱和食盐水的方式收集氯气 | |
| C. | 打开汽水瓶,有气泡从溶液中冒出 | |
| D. | 对熟石灰的悬浊液加热,悬浊液中固体质量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
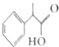 所示.
所示.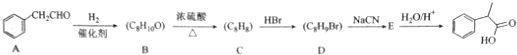
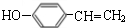 .
.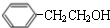 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$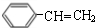 +H2O;C→D的反应类型为加成反应.
+H2O;C→D的反应类型为加成反应.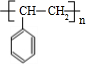 .
.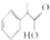 )的叙述正确的是B(填字母序号)
)的叙述正确的是B(填字母序号)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCN的结构式:H-C≡N | |
| B. | HClO的电子式: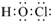 | |
| C. | 中子数为16的硫原子符号为:${\;}_{32}^{16}$S | |
| D. | Na+的离子结构示意图: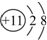 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgCl2(熔融) $\frac{\underline{\;电解\;}}{\;}$ Mg+Cl2↑ | B. | Al2O3+3C $\frac{\underline{\;2125℃\;}}{\;}$2Al+3CO↑ | ||
| C. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | HgS+O2$\frac{\underline{\;焙烧\;}}{\;}$ Hg+SO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
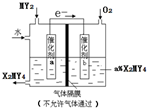 X、Y、Z、M、Q是五种短周期主族元素,原子序数依次增大.X、Y可形成最常用溶剂;X、Y、Z最外层电子数之和为8;Y、M形成的气态化合物在标准状况下的密度为2.86g•L-1.请回答下列问题:
X、Y、Z、M、Q是五种短周期主族元素,原子序数依次增大.X、Y可形成最常用溶剂;X、Y、Z最外层电子数之和为8;Y、M形成的气态化合物在标准状况下的密度为2.86g•L-1.请回答下列问题: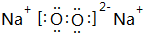 ;将A加入盛有酚酞试液的试管中观察到的现象为有大量气泡生成,溶液先变红后褪色,发生反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
;将A加入盛有酚酞试液的试管中观察到的现象为有大量气泡生成,溶液先变红后褪色,发生反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
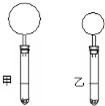 右下图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙完全反应后,所观察到的实验现象(反应过程中产生的气体全部收集在试管上部的气球中).下列说法不正确的是( )
右下图是10mLpH均为2的盐酸和醋酸分别与足量的碳酸钙完全反应后,所观察到的实验现象(反应过程中产生的气体全部收集在试管上部的气球中).下列说法不正确的是( )| A. | 乙试管中盛放的是盐酸溶液 | |
| B. | 甲试管中盛放的是醋酸溶液 | |
| C. | 反应开始时的速率:甲>乙 | |
| D. | 反应结束时消耗碳酸钙的质量:甲>乙 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com