
【题目】高温下可将煤转化为水煤气,水煤气可作为气体燃料,有关热化学方程式如下:
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=+131.3 kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ/mol
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ/mol
下列说法正确的是
A. 煤不属于化石燃料
B. 等质量的CO和H2完全燃烧时,前者放热多
C. 水煤气作为气体燃料,比煤直接燃烧污染小
D. 由反应③可以确定H2的燃烧热为241.8 kJ/mol
科目:高中化学 来源: 题型:
【题目】现有NH4Cl、(NH4)2SO4和K2SO4三种无色溶液,只用一种试剂,一次区别开,则该试剂是(必要时可以加热)( )
A. BaCl2溶液 B. Ba(OH)2溶液 C. 稀盐酸 D. AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,分别向10 mL浓度均为0.1mol/L的CuCl2和ZnCl2溶液中滴加0.1mol/L的Na2S 溶液,滴加过程中溶液中-1gc(Cu2+)和-lgc(Zn2+)与Na2S 溶液体积(V)的关系如图所示。(已知: Ksp(ZnS) > Ksp(CuS),1g3≈0.5) 下列有关说法错误的是
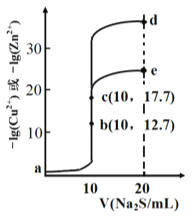
A. 溶液pH:a<b<e B. a 点的ZnCl2 溶液中: c(Cl-)<2[c(Zn2+)+c(H+)]
C. a-b-e为滴定CuCl2溶液的曲线 D. d点纵坐标小于34.9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四只盛有不同溶液的烧杯中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发):

则下列分析都正确的组合是( )
①I图对应溶液中的溶质为NaHCO3
②II图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1:1
③III图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1
④IV图对应溶液中的溶质为Na2CO3
A.①② B.①③ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲和乙为中学化学常见金属单质,丙和丁为常见气体单质,A~E为常见化合物;A为淡黄色固体,常温下B为液体,C的焰色反应为黄色。试回答下列问题:
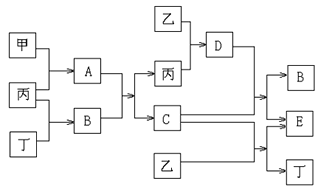
(1)A和E的化学式分别为_____________、____________;
(2)A+B→C+丙的化学方程式:__________________________________________ ;
(3)D+C→B+E的化学方程式:__________________________________________ ;
(4)1mol甲和1mol乙混合投入到足量的B中,在标准状况下,最多能产生丁气体______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)①H2 + CuO ![]() Cu + H2O
Cu + H2O
②CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
③3S + 6NaOH ![]() 2Na2S + Na2SO3 + 3H2O
2Na2S + Na2SO3 + 3H2O
④NH4NO3 + Zn = ZnO + N2↑+ 2H2O
⑤Cu2O + 4HCl = 2HCuCl2 + H2O
上述反应中,属于氧化还原反应的是__________________________(填序号)
(2)SeO2、KI和HNO3可发生反应:SeO2+KI+HNO3→Se+I2+KNO3+H2O,配平该反应的化学方程式并用双线桥法标出电子转移的方向和数目:____________________________。
(3)在反应 KIO3 + 6HI = 3I2 + KI + 3H2O中,氧化剂与还原剂的物质的量之比为__________。
Ⅱ.已知:
① 2H2O + Cl2 + SO2 = H2SO4 + 2HCl ② 2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
(4)根据以上两个反应可以得出氧化剂和还原剂的强弱顺序,请写出由KMnO4、K2SO4 、MnSO4 、SO2、H2O、H2SO4 这六种物质组成的氧化还原反应的方程式并配平:_______________________。
在反应②中,若有18.25g HCl被氧化,求:
(5)转移的电子数为:_______________。
(6)标况下生成Cl2的体积(请列式计算)_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH4Al(SO4)2在食品、医药、电子工业中用途广泛。回答下列问题:
(1)NH4Al(SO4)2可做净水剂,其理由是____________________(用离子方程式表示)。
(2)相同条件下,0.1mol/LNH4Al(SO4)2溶液中,c(NH4+)_____0.1mol/LNH4HSO4溶液中c(NH4+)(填“大于”、“等于”或“小于”)。
(3)下图是0.1mol/L 电解质溶液的pH 随温度变化的图像。

①其中符合0.1mol/LNH4Al(SO4)2溶液的是________(填字母)。导致溶液pH随温度变化的原因是_____________________________。
②20℃时,0.1mol/LNH4Al(SO4)2溶液中,2c(SO42-)-c(NH4+) -3c(Al3+)=_____mol/L。
(4)室温时,向0.1mol/LNH4Al(SO4)2溶液中滴加0.1mol/LNaOH 溶液。得到溶液pH与NaOH溶液体积关系曲线如图所示:
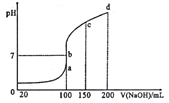
①已知:Ksp[Al(OH)3]=1×10-33,Al3+沉淀完全时(使其浓度小于1×10-6mol·L-1),溶液的pH=_______,试分析图中a、b、c、d四点,水的电离程度最大的是______________________。
②在b点,溶液中各离子浓度由大到小的顺序是_______________。
③b-c段随着NaOH的加入,溶液中c(NH3·H2O)/c(OH-)的值_____(填“增大”、“减小”或 “不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com