
(10分)A、B、C、D、E都是短周期元素,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D元素在周期表中的位置是 乙物质的电子式是__________
(2)A、B、C、D、E五种元素的原子半径由小到大的顺序是_________ (用元素符号填写)
(3)E的单质加入到C的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是
(4)E的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,其中有一种产物是TiC(在火箭和导弹上有重要应用)其反应方程式为
科目:高中化学 来源:2013-2014江苏省南通市高三第三次调研测试化学试卷(解析版) 题型:实验题
(14 分) 一氧化碳被广泛应用于冶金工业和电子工业。
⑴高炉炼铁是最为普遍的炼铁方法,相关反应的热化学方程式如下:
4CO(g)+Fe3O4(s)=4CO2(g)+3Fe(s) △H=a kJ·mol-1
CO(g)+3Fe2O3(s)=CO2(g)+2Fe3O4(s) △H=b kJ·mol-1
反应3CO(g)+Fe2O3(s)=3CO2(g)+2Fe(s)的△H= kJ·mol-1(用含a、b 的代数式表示)。
⑵电子工业中使用的一氧化碳常以甲醇为原料通过脱氢、分解两步反应得到。
第一步:2CH3OH(g) HCOOCH3(g)+2H2(g) △H>0
HCOOCH3(g)+2H2(g) △H>0
第二步:HCOOCH3(g) CH3OH(g) +CO(g) △H>0
CH3OH(g) +CO(g) △H>0
①第一步反应的机理可以用下图表示:
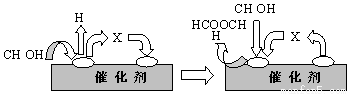
图中中间产物X的结构简式为 。
②在工业生产中,为提高CO的产率,可采取的合理措施有 。
⑶为进行相关研究,用CO还原高铝铁矿石,反应后固体物质的X—射线衍射谱图如图所示(X—射线衍射可用于判断某晶态物质是否存在,不同晶态物质出现衍射峰的衍射角不同)。反应后混合物中的一种产物能与盐酸反应生产两种盐,该反应的离子方程式为 。

⑷某催化剂样品(含Ni2O340%,其余为SiO2)通过还原、提纯两步获得镍单质:首先用CO将33.2 g样品在加热条件下还原为粗镍;然后在常温下使粗镍中的Ni与CO结合成Ni(CO)4(沸点43 ℃),并在180 ℃时使Ni(CO)4重新分解产生镍单质。
上述两步中消耗CO的物质的量之比为 。
⑸为安全起见,工业生产中需对空气中的CO进行监测。
①粉红色的PdCl2溶液可以检验空气中少量的CO。若空气中含CO,则溶液中会产生黑色的Pd沉淀。每生成5.3gPd沉淀,反应转移电子数为 。
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其结构如图所示。这种传感器利用原电池原理,则该电池的负极反应式为 。

查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市高一下学期期末学情调研测试化学试卷(解析版) 题型:填空题
(10分)信息时代产生的大量电子垃圾对环境构成严重威胁。某研究性学习小组将一批废弃的线路板简单处理后,得到含Cu、Fe及少量Au、Pt等金属的混合物,并用如下流程制备胆矾晶体(CuSO4?5H2O):

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Cu2+ |
开始沉淀 | 1.5 | 6.4 | 4.2 |
完全沉淀 | 3.2 | 8.9 | 6.7 |
(1)滤渣Ⅰ的主要成份是(写化学式)______。
(2)反应Ⅱ中加入H2O2的作用是______。
(3)沉淀过程中发生反应的离子方程式有______、______。
(4)操作Ⅰ的步骤是______、______、过滤、洗涤、干燥。
(5)测定胆矾晶体纯度的实验步骤如下:
a. 准确称取3.125g胆矾晶体样品配成100mL溶液;
b. 取10.00 mL溶液于带塞锥形瓶中,加适量水稀释,加入过量KI固体,发生反应:
2Cu2+ +4Iˉ= 2CuI↓ + I2
c. 继续向上述混合物中,逐滴加入0.1000 mol·L-1Na2S2O3溶液至恰好完全反应,共消耗12. 00mL Na2S2O3溶液:I2+2S2O = 2Iˉ+S4O
= 2Iˉ+S4O
求样品中胆矾晶体的质量分数(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市高一下学期期末学情调研测试化学试卷(解析版) 题型:选择题
煤燃烧的烟气中含有CO和SO2气体,下列关于这两种气体的说法正确的是
A.两者都易溶于水
B.两者都是有毒气体
C.两者都能使品红溶液褪色
D.两者都是形成酸雨的主要原因
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市高一下学期期末学情调研测试化学试卷(解析版) 题型:选择题
医疗上给病人输液补充能量,常用的糖是
A.葡萄糖 B.麦芽糖 C.淀粉 D.纤维素
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
经测定由C3H7OH和C6H12组成的混合物中氧的质量分数为8%,则此混合物中氢的质量分数是
A.78% B.22% C.14% D.13%
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
下列过程发生了化学反应的是
A.用自来水制蒸馏水 B.从海水中获得氯化钠
C.煤的干馏 D.石油的分馏
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省南京市雨花区高一下学期期末考试化学试卷(解析版) 题型:选择题
放射性同位素铀 的原子核内的中子数是
的原子核内的中子数是
A.51 B.92 C.143 D.235
查看答案和解析>>
科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:填空题
(6分)按下图装置进行实验,回答下列问题(C、C1、C2均为石墨电极)。

(1)铁电极为__________极,电极反应式为__________;
(2)石墨棒C1为__________极,石墨棒C2附近的实验现象为____________________。
(3)当C2极产生2.24 L气体(标准状态)时,A中CuSO4溶液的质量改变了__________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com