
【题目】下列离子方程式正确的是( )
A. 二氧化硅溶于氢氟酸溶液中: SiO2+4H++4F-![]() SiF4↑ +2H2O
SiF4↑ +2H2O
B. 钠加入水中:2Na + 2H2O![]() 2Na+ + 2OH- + H2↑
2Na+ + 2OH- + H2↑
C. 稀硫酸加入氢氧化钡溶液中:H+ +![]() + Ba2+ + OH-
+ Ba2+ + OH-![]() BaSO4↓+ H2O
BaSO4↓+ H2O
D. 铜加入氯化铁溶液中:Cu+Fe3+![]() Cu2+ + Fe2+
Cu2+ + Fe2+
科目:高中化学 来源: 题型:
【题目】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度。(A中可供选用的试剂只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)
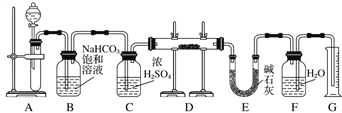
回答下列问题:
(1)装置A中液体试剂选用________ ,A中发生反应的离子方程式为______________。
(2)装置B的作用是________________。装置E中碱石灰的作用是_________________。
(3)装置D中发生反应的化学方程式_________________ , _____________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去苯中所含的苯酚,可采用的适宜方法是( )
A.加70℃以上的热水,分液
B.加适量浓溴水,过滤
C.加足量NaOH溶液,分液
D.加适量FeCl3溶液,过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.5L 1mol/L FeCl3溶液与0.2L1mol/L KCl溶液中的Cl-的数目之比
A. 5:2 B. 3:1 C. 15:2 D. 1:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,并放出X kJ热量.已知单质C(s)的燃烧热为Y kJ/mol,则1mol C(s)与O2(g)反应生成CO(g)的反应热△H为( )
A.﹣Y kJ/mol
B.﹣(10X﹣Y)kJ/mol
C.﹣(5X﹣0.5Y) kJ/mol
D.+(10X﹣Y)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质(或离子)均含有同一种元素,它们之间有如图所示的转化关系: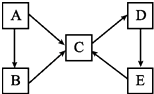
(1)若A为单质,C、D的相对分子质量相差16,0.05 molL﹣1 E溶液中只有3种离子,且在25℃时,溶液中的 ![]() =1012 . ①若B为气态氢化物,写出E→C的一个化学方程式 .
=1012 . ①若B为气态氢化物,写出E→C的一个化学方程式 .
②在A→C的反应中,每转移1 mol e﹣就会放热143.5 kJ,写出该反应的热化学方程式 .
(2)若A为单质,B、C均属于盐类,D是一种白色沉淀.①若B的水溶液呈酸性,C的水溶液呈碱性,C溶液呈碱性的原因是(用离子方程式表示).
②若B溶液呈黄色,与硫氰化钾溶液混合后显红色,E是一种不溶性碱.则:
(Ⅰ)B→C的离子方程式为 .
(Ⅱ)D→E的化学方程式为 .
(Ⅲ)选用一种试剂R与E反应实现E→C的转化,则R为;该反应的离子方程式为 .
(3)若A~E均为化合物,且均含有元素Y.A是淡黄色固体,B、C两溶液在等物质的量浓度时,C溶液的pH较小.电解D的水溶液是最重要的工业生产之一,D→E→C也是工业制备C的普遍方法.Y的单质与钾的合金可在核反应堆中用作热交换液.5.05 g Y钾合金溶于200 mL水生成0.075 mol氢气,计算并确定该Y钾合金的化学式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于加成反应的是( )
A.乙烯使酸性KMnO4溶液褪色
B.将苯滴入溴水中,振荡后水层接近无色
C.乙烯使溴的四氯化碳溶液褪色
D.甲烷与氯气混合,光照一段时间后黄绿色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室可用KMnO4和浓盐酸反应制取氯气。
2KMnO4+16HCl(浓) ![]() 2KCl+2MnCl2+5Cl2↑+8H2O
2KCl+2MnCl2+5Cl2↑+8H2O
(1)用单线桥标出电子转移的方向和数目。____________________
(2)将上述配平的化学方程式改写为离子方程式__________________________________ 。
(3)浓盐酸在反应中显示出来的性质是________________
①只有还原性 ②还原性和酸性
③只有氧化性 ④氧化性和酸性
(4)若产生0.5molCl2,则被氧化的HCl________mol,转移的电子的数目约为____________。
II.根据反应Cu+4HNO3(浓)![]() Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原产物是______。
②氧化剂与氧化产物的物质的量之比是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体摩尔体积的描述中正确的是( )
A. 气体摩尔体积的数值是固定不变的,都约为22.4L
B. 通常状况下的气体摩尔体积约为22.4L
C. 标准状况下的气体的摩尔体积约为22.4L
D. 标准状况下,气体的摩尔体积约为22.4L/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com