
����Ŀ��������װ�ô�����KMnO4�ķ�Һ��ʹMnԪ��ת��ΪMnO2�������Ӷ������ؽ�����Ⱦ������˵���������
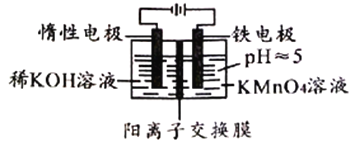
A. MnO4-������ȫ��ʵ�����ʱ�����ܻ����ɳ���
B. �Ҳ������Fe2+����MnO4-�����ӷ���ʽΪ��7H2O+3Fe2++MnO4-=3Fe(OH)3��+MnO2��+5H+
C. ����·��ת��6mole-ʱ�����Բ���87gMnO2����
D. Ϊ�������Ҳ���Һ�ĵ����Կ��Լ�ϡ�������ǿ���Ի���
���𰸡�D
���������������������Ⲣ���ͼʾ�����缫Ϊ���ص�����������������Ӧ����Fe2+����������������Fe2+��MnO4-����������ԭ��ӦʹMnԪ��ת��ΪMnO2������
��⣺A�MnO4-������ȫ���������ɵ�Fe2+��ͨ�������ӽ���Ĥ������࣬����������Fe(OH)2��������A��ȷ��B��Ҳ������Fe2+�������������½�MnO4-��ԭΪMnO2������������ΪFe(OH)3���������ӷ���ʽΪ��7H2O+3Fe2++MnO4-=3Fe(OH)3��+MnO2��+5H+����B��ȷ��C����������缫��Ӧ��Fe-2e-=Fe2+������·��ת��6mole-ʱ������3molFe2+������Fe2+����MnO4-�����ӷ���ʽ7H2O+3Fe2++MnO4-=3Fe(OH)3��+MnO2��+5H+�ɵã�����1molMnO2������Ϊ��1mol��87g/mol=87g����C��ȷ��D�ǿ������������MnO4-��Fe2+��ӦΪ��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O������ʹMnԪ��ת��ΪMnO2��������D�������Ϸ��������������ѡ��ΪD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����t ��ʱ����x g KNO3��������Һ�м���a g KNO3��������b gˮ���ָ���t ������Һ���ﵽ���ͣ��ݴˣ��������۲���ȷ����( )
A. ��t ��ʱ��KNO3���ܽ��Ϊ![]() g
g
B. ��ԭ��Һ�����ʵ���������Ϊ![]() ����x=2b
����x=2b
C. ��t ��ʱ�������KNO3��Һ�����ʵ���������Ϊw��![]() %
%
D. ����ԭ��Һ������2b gˮ���ָ���ԭ�¶�����2a g KNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���黯���Ǽ̹�֮���о������롢Ӧ����㷺�İ뵼����ϡ��ش�����������
��1��Ga��̬ԭ�Ӻ�������Ų�ʽΪ__________________��As��̬ԭ�Ӻ�����____��δ�ɶԵ��ӡ�
��2��Ga��As��Se�ĵ�һ�������ɴ�С��˳����___________��Ga��As��Se�ĵ縺���ɴ�С��˳����_________________��
��3���Ƚ������ص�±������۵�ͷ�㣬������仯���ɼ�ԭ����_________________��
�ص�±���� | GaI3 | GaBr3 | GaCl3 |
�۵�/�� | 77.75 | 122.3 | 211.5 |
�е�/�� | 201.2 | 279 | 346 |
GaF3���۵㳬��1000�������ܵ�ԭ����______________��
��4����ˮ�ϲ����صĽṹ��ͼ1��ʾ��������ԭ�ӵ���λ��Ϊ___________���������̼ԭ�ӵ��ӻ��������Ϊ______________��

��5���黯�ص����������ṹ��ͼ2��ʾ����������Ϊa=0.565nm���黯�ؾ�����ܶ�Ϊ_____g/cm3(��NAΪ�����ӵ�������ֵ���г�����ʽ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��·�Ӧ��A2��g��+3 B2��g��![]() 2 AB3��g�� ��ÿ����2 mol AB3�ų�92.4 kJ�����������ں��º�ѹ���ܱ������н�������ʵ�飺��ͨ��1 mol A2��3 mol B2����ƽ��ʱ�ų�����ΪQ1����ͨ��2 mol A2��6 mol B2����ƽ��ʱ�ų�����ΪQ2�������й�ϵ��ȷ����
2 AB3��g�� ��ÿ����2 mol AB3�ų�92.4 kJ�����������ں��º�ѹ���ܱ������н�������ʵ�飺��ͨ��1 mol A2��3 mol B2����ƽ��ʱ�ų�����ΪQ1����ͨ��2 mol A2��6 mol B2����ƽ��ʱ�ų�����ΪQ2�������й�ϵ��ȷ����
A��Q2 = 2 Q1 B��2Q1 < Q2
C��Q1 < Q2 < 92.4 kJ D��Q1 = Q2 < 92.4 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ksp(AgCl)=1.56��10-10��Ksp(AgBr)=7.7��10-13��Ksp(Ag2CrO4)=9.0��10-11��ij��Һ�к���Cl-��Br-��CrO42-��Ũ�Ⱦ�Ϊ0.010mol/L�������Һ����μ���0.010mol/L��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
A. Cl-��Br-��CrO42- B. CrO42-��Br-��Cl-��
C. Br-��Cl-��CrO42- D. Br-��CrO42-��Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ת����ϵ�ж�����˵����ȷ���ǣ���Ӧ��������ȥ����������
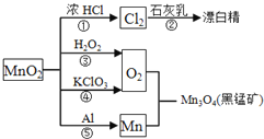
A. ��Ӧ�٢ڢۢܢ�������������Ӧ�����ӷ�Ӧ
B. ��Ӧ��˵�������������Ļ�ԭ��ǿ����
C. ��ͬ���������ɵ�����O2����Ӧ������ת�Ƶĵ�����֮��Ϊ1�U1
D. ��Ӧ�����������뻹ԭ�������ʵ���֮��Ϊ1�U4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ĺ�ҵԭ�ϡ�
��1��д��ʵ������ȡ������Ӧ�Ļ�ѧ����ʽ________________________��
��2��������ʾ��Ca(ClO)2 +CaCl2+2H2SO4![]() 2CaSO4+2Cl2��+2H2O��ijѧϰС�����ô�ԭ�������ͼ��ʾװ����ȡ������̽�������ʡ�
2CaSO4+2Cl2��+2H2O��ijѧϰС�����ô�ԭ�������ͼ��ʾװ����ȡ������̽�������ʡ�
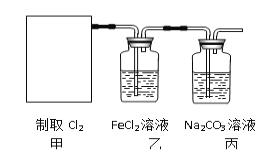
���ڸ�ʵ���У��ײ��ֵ�װ����_______������ĸ����
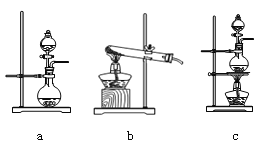
����װ����FeCl2��Һ��Cl2��Ӧ�����ӷ���ʽ��________________��
����װ����ͨ������Cl2�����Ƶ�ij�������г��õ�Ư�ס����������ʣ�����������_______����ѧʽ����
��������Ϊ��ʵ��������Ե�ȱ�ݣ���θĽ���______________
����д��Cl2�����ܡ���������ʵĻ�ѧ�Լ�����Ӧ�����ӷ���ʽ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת������Ҫ���뻹ԭ������ʵ�ֵ���
A.SO3��H2SO4B.Cu��Cu(NO3)2C.Fe2O3��FeD.CO��CO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com