
| A. | 16O和18O | B. | H2O和D2O | C. | 金刚石和石墨 | D. | 24Mg和24Na |
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案科目:高中化学 来源: 题型:选择题
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,加铜片和浓硫酸加热 | 有无色气体产生,气体遇空气可以变成红棕色 |
| (2)取少量该溶液,加BaCl2溶液 | 有白色沉淀产生 |
| (3)取(2)中上层清液,加AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于硝酸 |
| (4)取少量该溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀溶解 |
| A. | 一定含有NO3-、SO42-和Cl- | |
| B. | 一定含有Al3+,可能含有Ba2+ | |
| C. | 一定含有NO3-、SO42-,可能含有HCO3- | |
| D. | 一定不含Fe2+、Ba2+和HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:
如图所示,隔板Ⅰ固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:| A. | 若x:y=1;2,则平衡时,M中的转化率:N2>H2 | |
| B. | 若x:y=1:3,当M中放出热量172.8kJ时,N2的转化率为90% | |
| C. | 若x=1,y=3,则达到平衡时反应物的转化率N>M | |
| D. | 平衡时N2气体在两容器中体积分数可能相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | n=1,l=1 m=0 | B. | n=2,l=0 m=±1 | C. | n=3,l=3 m=±3 | D. | n=4,l=3 m=±2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 “诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图,下列关于“诺龙”的说法中不正确的是( )
“诺龙”属于国际奥委会明确规定的违禁药品中合成代谢类的类固醇,其结构简式如图,下列关于“诺龙”的说法中不正确的是( )| A. | 既能发生加成反应,也能发生酯化反应 | |
| B. | 既能发生氧化反应,也能发生还原反应 | |
| C. | 分子式是C18H26O2 | |
| D. | 能在NaOH醇溶液中发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
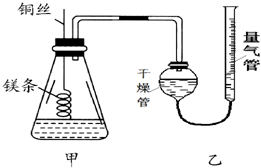 某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:
某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com