
����Ŀ����������������Ӧ����㷺�����������ͺ����²��ϵ�Ӧ�ñ��ܹ�ע��
(1)��¯������ұ��������Ҫ��������������Ҫ��Ӧ��:
��Ӧ | ��H(kJ/mol) | K |
i. Fe2O3(s)+3C(s) | +489 | K1 |
ii. Fe2O3(s)+3CO(g) | X | K2 |
iii. C(s)+CO2(g) | +172 | K3 |
�Լ��㣬X=_____��K1��K2��K3֮��Ĺ�ϵΪK1=__________��
(2)T1��ʱ,��ij�����ܱ������м���һ������Fe2O3��C��������Ӧi����Ӧ�ﵽƽ�����t1ʱ��,�ı�ij����,V(��)��ʱ��(t)�ı仯��ϵ��ͼ1��ʾ����t1ʱ�̸ı������������_____(��д��ĸ)��
a.�����¶Ȳ���,ѹ������ b.����������䣬�����¶�
c.�����������,������̼�� d.�����������,����COŨ��
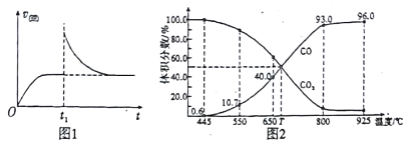
(3)��һ���¶��£���ij����ɱ�ĺ�ѹ�ܱ�����(p��)����1molCO2 ��������̼��������Ӧ����ƽ��ʱ��ϵ����������������¶ȵĹ�ϵ��ͼ2 ��ʾ��
��650��ʱ,�÷�Ӧ��ƽ������յ�������_________��
��T��ʱ,����ƽ����ϵ���ٳ���һ������V(CO2):V(CO) =5:4�Ļ�����壬ƽ��_____(� ������ ���� ���� )�ƶ���
��925��ʱ,��ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��KpΪ_____��[�����ѹ(p��)=������ѹ(p��) �������������ij���ʵ�ƽ���ѹ�������ʵ���Ũ��Ҳ���Ա�ʾ��ѧƽ�ⳣ��������Kp]
(4)��ԭ���ԭ�����Գ�ȥ���Է�ˮ�е�������ϩ��AsO3-����ԭ������ͼ��ʾ( ������ڲ�Ϊ���������)��
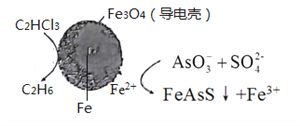
�ڳ��۹����У�����������е�FeΪԭ��ص�______�� (���"����)��д��C2HCl3������汻��ԭΪ����ĵ缫��ӦʽΪ_____________��
���𰸡�-27 K2K33 ad 43kJ ���� 23.04P�� �� C2HCl3 +5H++8e-=C2H6 +3Cl-
��������
��֪��i. Fe2O3(s)+3C(s)![]() 2Fe(s)+3CO(g) ��H=+489 kJ/mol��K1=c3(CO)��iii. C(s)+CO2(g)
2Fe(s)+3CO(g) ��H=+489 kJ/mol��K1=c3(CO)��iii. C(s)+CO2(g) ![]() 2CO(g) ��H=+172 kJ/mol��K3= c2(CO)/C(CO2)����i- iii
2CO(g) ��H=+172 kJ/mol��K3= c2(CO)/C(CO2)����i- iii![]() 3�ã�Fe2O3(s)+3CO(g)
3�ã�Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) ��H=+489-172
2Fe(s)+3CO2(g) ��H=+489-172![]() 3=-27 kJ/mol;K2= c3(CO2)/ c3(CO)��K2. K33=[c3(CO2)/ c3(CO)] [c2(CO)/C(CO2)]3= c3(CO)=K1���𰸣� -27 K2K33
3=-27 kJ/mol;K2= c3(CO2)/ c3(CO)��K2. K33=[c3(CO2)/ c3(CO)] [c2(CO)/C(CO2)]3= c3(CO)=K1���𰸣� -27 K2K33
�� Fe2O3(s)+3C(s) ![]() 2Fe(s)+3CO(g) ��H=+489 kJ/mol��ͼ1�淴Ӧ����Ѹ�������淴Ӧ����a.�����¶Ȳ���,ѹ������,�൱������CO��Ũ�ȣ������淴ӦѸ������������a�������⣻b.����������䣬�����¶�ƽ�������ƶ������淴Ӧ���ʶ�����ѧƽ�ⳣ���������b���������⣻c.�����������,������̼�ۣ���Ϊ̼���ǹ��壬�ı���������Ӱ�컯ѧƽ���ƶ�������c���������⣻d.�����������,����COŨ�ȣ�����������Ũ�ȣ����淴Ӧ���ʶ������淴Ӧ�������ӵ����ʸ��죬���¶�û�䣬��ѧƽ�ⳣ�����䣬����d�������⣻�𰸣�.ad��
2Fe(s)+3CO(g) ��H=+489 kJ/mol��ͼ1�淴Ӧ����Ѹ�������淴Ӧ����a.�����¶Ȳ���,ѹ������,�൱������CO��Ũ�ȣ������淴ӦѸ������������a�������⣻b.����������䣬�����¶�ƽ�������ƶ������淴Ӧ���ʶ�����ѧƽ�ⳣ���������b���������⣻c.�����������,������̼�ۣ���Ϊ̼���ǹ��壬�ı���������Ӱ�컯ѧƽ���ƶ�������c���������⣻d.�����������,����COŨ�ȣ�����������Ũ�ȣ����淴Ӧ���ʶ������淴Ӧ�������ӵ����ʸ��죬���¶�û�䣬��ѧƽ�ⳣ�����䣬����d�������⣻�𰸣�.ad��
(3) ����ͼ2��֪��650��ʱ��Ӧ��ƽ���CO���������Ϊ40![]() �����ݻ�ѧƽ������ʽ�ɣ�
�����ݻ�ѧƽ������ʽ�ɣ�
C(s)+CO2(g) ![]() 2CO(g) ��H=+172 kJ/mol
2CO(g) ��H=+172 kJ/mol
��ʼ�� (mol) 1 0
�仯����mol�� x 2x
ƽ������mol�� 1-x 2x
�� [2x/(1-x+2x)]![]() 100
100![]() =40
=40![]() ,x=0.25mol�������Ȼ�ѧ��Ӧ����ʽ֪�÷�Ӧ�ﵽƽ��ʱ���յ�����Ϊ0.25mol
,x=0.25mol�������Ȼ�ѧ��Ӧ����ʽ֪�÷�Ӧ�ﵽƽ��ʱ���յ�����Ϊ0.25mol![]() 172 kJ/mol=43kJ���𰸣�43kJ��
172 kJ/mol=43kJ���𰸣�43kJ��
��T��ʱ,����ƽ����ϵ���ٳ���һ������V(CO2):V(CO) =5:4�Ļ�����壬��ԭƽ��ʱV(CO2):V(CO) =1:1���簴V(CO2):V(CO) =5:4�൱��������c(CO2)Ũ�ȣ���ѧƽ�������ƶ����𰸣�������
��925��ʱ,CO���������Ϊ96![]() ����CO2���������Ϊ4
����CO2���������Ϊ4![]() ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=��96
����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��Kp=��96![]() P����2/(4
P����2/(4![]() P��)=23.04P�����𰸣�23.04P��
P��)=23.04P�����𰸣�23.04P��
��4����ͼ3֪�����������Feʧ������������C2HCl3������汻��ԭΪ���飬���ݵ���غ�͵����غ㣬�õ缫��ӦʽΪC2



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�ܱ��ݻ��������н��з�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2 molL-1��0.1 molL-1��0.2 molL-1������Ӧ��ƽ��ʱ�����ܴ��ڵ�������
2SO3(g)����֪��Ӧ������ijһʱ��SO2��O2��SO3��Ũ�ȷֱ�Ϊ0.2 molL-1��0.1 molL-1��0.2 molL-1������Ӧ��ƽ��ʱ�����ܴ��ڵ�������
A. SO2Ϊ0.4 molL-1��O2Ϊ0.2 molL-1 B. SO2Ϊ0.25 molL-1
C. SO2��SO3��Ϊ0.15 molL-1 D. SO3Ϊ0.4 molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ʯī�ͽ��ʯȼ�ջ�ѧ����ʽ���£�
C��ʯī��s��+O2��g��==CO2��g��
C�����ʯ��s��+O2��g��==CO2��g��
�����ֱ�Ϊ12 g��ʯī�ͽ��ʯ��ijһ��ͬ������ȼ��ʱ�ų��������ֱ�Ϊ393.8 kJ��395.2 kJ���ʣ����ڵ�����˵���ȶ��ĵ�����ʯī���ǽ��ʯ���������ɡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼�Ȼ�ԭ�Ʊ����������ܷ�Ӧ��ѧ����ʽΪ��Al2O3(s)+3C(s)+N2(g)![]() 2AlN(s)+3CO(g)�����¶ȡ��ݻ��㶨�ķ�Ӧ��ϵ�У�COŨ����ʱ��ı仯��ϵ��ͼ������ʾ������˵������ȷ����
2AlN(s)+3CO(g)�����¶ȡ��ݻ��㶨�ķ�Ӧ��ϵ�У�COŨ����ʱ��ı仯��ϵ��ͼ������ʾ������˵������ȷ����

A. �ڲ�ͬʱ�̶����ڹ�ϵ��v(N2)=3v(CO)
B. c�����ߵ�б�ʱ�ʾ�û�ѧ��Ӧ��tʱ�̵�˲ʱ����
C. ��a��b�����������ô�a��bʱ�����ڸû�ѧ��Ӧ��ƽ������
D. ά���¶ȡ��ݻ����䣬������N2�����ʵ������з�Ӧ������ת��Ϊ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ݻ�Ϊ3L���ܱ������ڽ������·�Ӧ��A2������+3B2������===aX����������Ӧ��ʼʱ��n(A2)=1.5mol��n(B2)= 4.0mol��2min��n(B2)=0.4mol�� n(X)=2.4mol�����㣺
��1��aֵ______________
��2��X�ı�ʾʽ����A��B��ʾ��________________
��3����(B2)Ϊ_____________
��4��2minĩ��A2��Ũ��_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼΪ̽�ֱ�����ķ�Ӧ�Ľ���ʵ��װ��ͼ������AΪ��֧�Թܸ��Ƴɵķ�Ӧ�����������¶˿���һ��С�ף�������ʯ���ޣ�ʵ��ʱ�ȼ�����������ʯ�����ϡ���д���пհף�
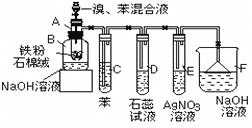
��1����Ӧ����A����μ�����ͱ��Ļ��Һ���������ڷ�����Ӧ��д��A����������Ӧ�Ļ�ѧ����ʽ____��______��
��2����Ӧ��ʼ��۲�D��E���Թܣ�����������Ϊ____��_____��˵������Һ�巢����__��Ӧ��
��3��C�б���������____��F��NaOH��Һ��������____��
��4������������װ���У����з�������������F���____(����ĸ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ȡ��������ϩʱ���������Ҵ���Ũ������ټ��ȵ�170������ȡ����ʵ�鳣���¶ȹ��߶���������Ӧ���в����Ҵ���ŨH2SO4��Ӧ����SO2��C02��ˮ������̿�ڡ�
I���÷���ʽ��ʾ��ϩ�Ʊ��ķ�Ӧԭ��____����ϩ�Ʊ�ʱ����140�泣�����и���Ӧ��������ѧ����ʽΪ_____��
�������������ʵ����ȷ�������������������ϩ�Ͷ�������������������⣺
��1��ͼ�Т٢ڢۢ�װ�ÿ�ʢ�ŵ��Լ��ǣ��Լ����ظ�ʹ�ã�Ҳ�ɲ�ʹ�ã�������дABCD��
��_____����____����_____����______��
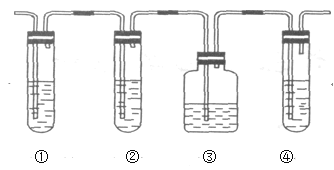
A��Ʒ����Һ B��NaOH��Һ C��ŨH2SO4 D������KMnO4��Һ
��2����˵����������������ڵ�������______��
��3��ʹ��װ�âڵ�Ŀ����___________��
��4��ʹ��װ�â۵�Ŀ����______________��
��5��ȷ֤������ϩ��������_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؼ����˵���д�����ǣ�������
A.���������������
B.���鼫������ˮ
C.������γɷ��Ӿ���
D.���³�ѹ�¼���Ϊ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CH4��C2H4��C2H6�����л��
(1)����������������������ȫȼ��ʱ��O2����������______�����ɵ�CO2����������______��
(2)ͬ״����ͬ�������������������ȫȼ��ʱ���ĵ�O2����������______��
(3)��120�棬1.01��105 Paʱ�������л����е����ֺ�������������ϵ�ȼ����ͬ�����²�÷�Ӧǰ���������û�з����仯��������������______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com