
分析 (1)X是一种硫酸盐,且0.2mol X在该反应中失去1mol 电子,即1molX在该反应中失去5mol电子,根据元素守恒知,该元素是锰元素,生成物中锰元素是+7价,则X中锰元素显+2价,所以X是MnSO4,根据氧化还原反应中得失电子数相等配平方程式;
(2)用浓盐酸代替硫酸,反应生成氯化铅、氯气和水.
解答 解:(1)X是一种硫酸盐,且0.1mol X在该反应中失去0.5mol 电子,即1molX在该反应中失去5mol电子,根据元素守恒知,该元素是锰元素,生成物中锰元素是+7价,则X中锰元素显+2价,所以X是MnSO4,根据氧化还原反应中得失电子数相等配平方程式,该反应方程式为:2MnSO4+5PbO2+2H2SO4=Pb(MnO4)2+4PbSO4+2H2O,
故答案为:2MnSO4+5PbO2+2H2SO4=Pb(MnO4)2+4PbSO4+2H2O;
(2)该反应体系中,若用浓盐酸代替硫酸,反应生成氯化铅、氯气和水,用离子方程式表示:PbO2+4H++2Cl-═Pb2++Cl2↑+2H2O;
故答案为:PbO2+4H++2Cl-═Pb2++Cl2↑+2H2O.
点评 本题考查了氧化还原反应方程式的配平,明确发生反应的实质熟悉氧化还原反应得失电子守恒、原子个数守恒规律是解题关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
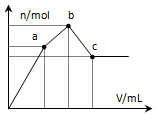 向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
向100mL 0.1mol•L-1硫酸铝铵溶液中逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A. | a点的溶液呈中性 | |
| B. | 从开始到b点发生反应的总的离子方程式是:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓ | |
| C. | c点加入Ba(OH)2溶液的体积为200 mL | |
| D. | c点溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.0mol.L-1的氨水中NH4+、NH3和NH3•H2O的总数为NA | |
| B. | 1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA | |
| C. | 0.1 mol Cu与足量浓硫酸反应生成SO2的体积约为4.48 L | |
| D. | 常温常压下,21g氧气和27 g臭氧所含的氧原子总数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| a | ||||
| b | ||||
| c | d | |||
| e |
| A. | b元素除0价外,只有一种化合价 | |
| B. | c元素只能形成一种氢化物且很不稳定 | |
| C. | d元素是五种元素中原子半径最小的一种 | |
| D. | e元素最高价氧化物的水化物和不同量的氢氧化钠溶液反应,可能生成三种盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MgO和Al2O3在工业上用于制作耐高温材料,也可用于电解法冶炼Mg、Al | |
| B. | 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质 | |
| C. | 高空臭氧层吸收太阳紫外线,保护地球生物;反应3O2═2O3有单质参加,属于氧化还原反应 | |
| D. | 向水中加入明矾进行杀菌消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丁一定是氧化剂 | B. | 甲只能是 S 或 N2 | ||
| C. | 乙一定是氧化物 | D. | 反应②可能是非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 5.4 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com